登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
中年女性,病程2个月,加重1个月。干咳、气促,胸部CT示双肺多发渗出性病灶,抗感染治疗效果差。患者的原发病究竟是感染性疾病还是非感染性疾病?后续需完善哪些检查?对于激素的使用,这一病例又将带给我们哪些启示?且看本期大查房回顾。
病情简介
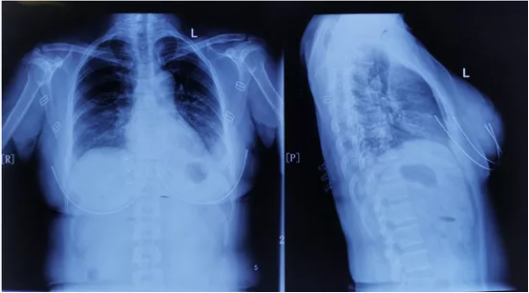
图1 患者胸部X线片(2020年5月14日)
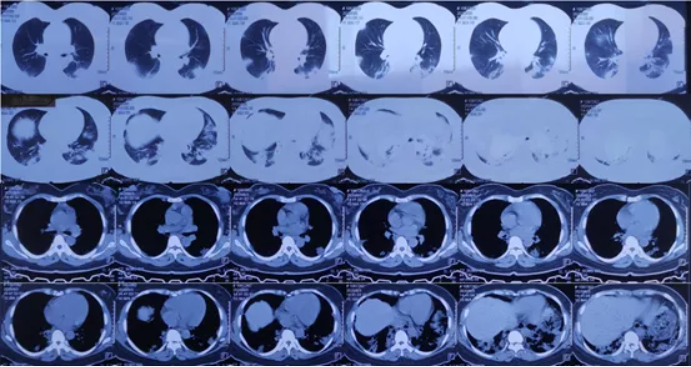
图2 患者胸部CT(2020年6月3日)
血常规:WBC 9.85×109/L,NEU% 80.80%,LYM% 13.40%,ESR、PCT、CRP正常。
病原学:G试验、GM试验、肺炎支原体IgM、肺炎衣原体IgM、甲流、乙流抗原、呼吸道病毒七种抗原、新冠核酸、结核抗体、HIV+TP、乙肝、丙肝均阴性。
结缔组织疾病:抗核抗体1:80(+)斑点型,SSA(+),类风湿因子18.2 U/L(↑),抗CCP、血管炎五项阴性。
肿瘤标志物:非小细胞肺癌抗原5.94 ng/ml(↑),NSE 18.17 ng/ml(↑)。
纤维支气管镜:会厌、气管、隆突均正常。右肺,1~4级支气管黏膜轻度发红,表面光滑,管腔通畅,可见稀薄分泌物,未见肿瘤或出血。左肺,1~4级支气管黏膜轻度发红,表面光滑,管腔通畅,可见稀薄分泌物,未见肿瘤或出血。于左肺下叶及右肺下叶基底段灌洗留取标本送检。镜下诊断:支气管炎症改变。
肺泡灌洗液:细菌涂片、真菌涂片、抗酸染色、细菌培养均阴性。
肺泡灌洗液NGS:真菌、病毒、寄生虫、结核、支原体/衣原体均阴性。
假单胞菌属(序列数277),铜绿假单胞菌(序列数46)。
嗜血杆菌属(序列数98),副流感嗜血杆菌(序列数86)。
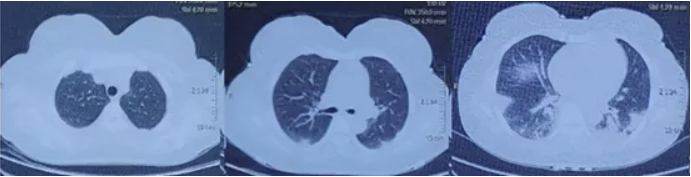
患者6月6日胸部CT较6月3日无明显变化,病变主要位于双下肺(图3)。
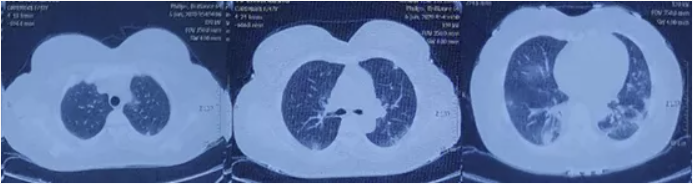
图3 患者胸部CT(2020年6月6日)
外院治疗
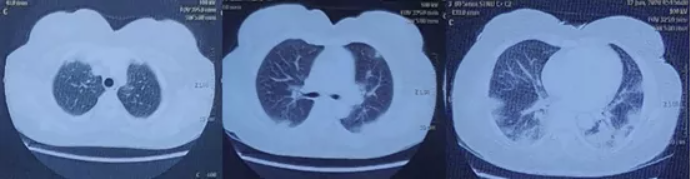
入我院诊治经过
专家讨论
从病史分析,中年女性,咳嗽2个月,渐进气喘,双下肺渗出病灶,呈锥形或楔形沿中央气道分布,导致胸膜下病变,病变较重部位有明显实变影,诊断方面考虑感染,当地医院给予常规抗感染治疗也是恰当的。之后根据放射科给出的COP的诊断可能,又给予了激素治疗,患者胸部影像学有所好转后出院,根据这一过程分析,COP的诊断也是准确的。但是患者自身免疫疾病相关指标存在异常,尤其是中年女性患者,SSA(+),类风湿因子水平升高,而且激素减量后症状加重,所以从治疗方面来讲,还应该恢复激素的充分治疗。另外,BALF中检测到副流感嗜血杆菌,在合并感染时应予以考虑,后续应有相关检查。病情加重源于激素减量,有无合并感染的问题,查体中双下肺湿啰音、纤支镜下见稀薄分泌物,如果有血性分泌物还应考虑肺外的问题。
该患者有特征性影像学改变,靠近胸膜下双侧病变,炎症指标(WBC、CRP)无明显增高,抗感染治疗效果欠佳。就感染相关肺部改变来说,可能是病毒感染;虽然也会有真菌(隐球菌)感染早期会出现靠近胸膜下的病变,但随着疾病进展,其影像学也会发生改变,与本例患者表现不太符合。就非感染性疾病而言,结缔组织疾病(如干燥综合征)引起的肺部改变需要进一步排查。另外还有两种疾病需要我们引起关注,单从影像学考虑,百草枯中毒早期也可出现靠近胸膜的影像学改变,但该患者无相关病史,可以排除;另外一种是嗜酸细胞增多症,但该患者目前尚无足够的证据支持这一诊断。
血常规:白细胞11.11×109/L,NEU% 75.6%。
尿常规、大便常规正常。
肝/肾功能、电解质、CK、CK-MB、凝血功能、NT-proBNP大致正常。
病原学:G试验、GM试验均正常;结核斑点试验阴性;肺炎军团菌抗体(LP-Ab)阳性(+),新冠肺炎核酸检测阴性。
结缔组织疾病:ENA,Ro-52(52 kDa)(+++),补体C3、C4、ANA、ANCA、血管炎三项、类风湿因子均正常。
肿瘤:非小细胞肺癌相关抗原-21 14.560 ng/ml(↑)。
彩超:心脏彩超示心内结构未见明显异常,左室收缩功能测值正常范围。下肢血管彩超示双下肢深静脉血流通畅。
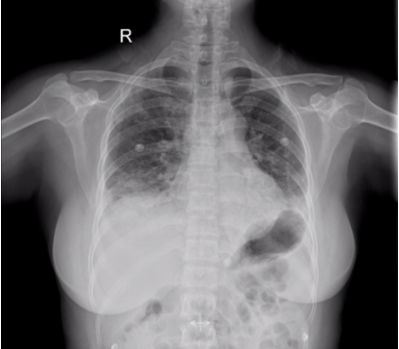
胸部X线片:7月23日患者胸部X线片可见右下肺渗出病灶较前明显加重(图6)。
纤支镜(7月23日):双侧支气管管腔通畅,未见肿块及出血。于右下外后基底支行肺活检。(支刷细胞块)少量纤毛柱状上皮细胞、淋巴细胞,未见典型癌细胞。(支气管刷/灌洗液)可见纤毛柱状上皮细胞、淋巴细胞、组织细胞,未见恶性肿瘤细胞。PAS(-)。
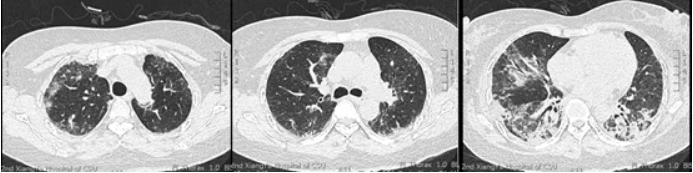
胸部CT:患者右上肺渗出病灶有少许增加(图7)。
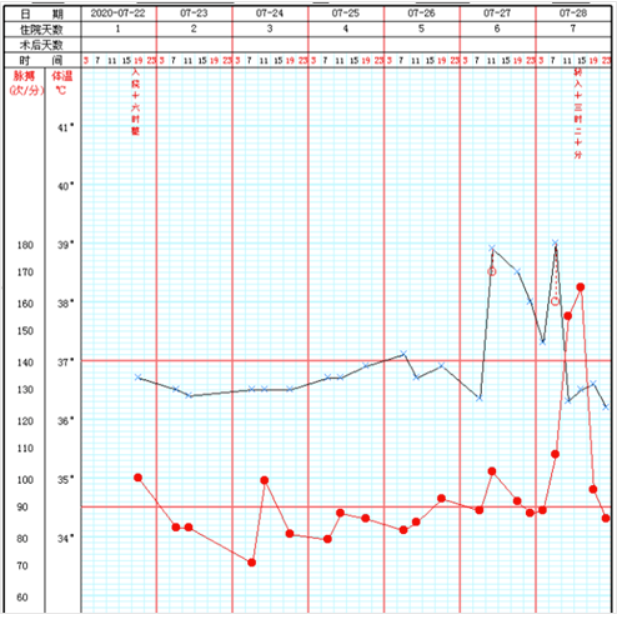
7月27日,患者出现发热,体温最高38.9°(图8)。
7月28日,血氧饱和度下降,气管插管,转入RICU。
T 36.5℃,P 165次/min,R 62次/min,BP 78/45 mmHg,血氧饱和度80%(气管插管呼吸机辅助呼吸:VCV模式,PEEP 3 cmH2O,FiO2 80%,VT 450 ml)。
神志清楚,查体不合作。浅表淋巴结未触及肿大。瞳孔等大等圆,对光反应敏感。口唇无发绀。胸廓对称,双肺叩诊为清音,双肺呼吸音粗,可闻及少量湿啰音。心前区无隆起,心界正常,心率170次/min,律绝对不齐,第一心音强弱不等,各瓣膜听诊未闻及病理性杂音。腹平软,无压痛及反跳痛,双下肢无水肿。病理反射未引出。
(有创机械通气,FiO2 100%)pH 7.358,PaCO2 38.0 mmHg,PaO2 102.0 mmHg,cLac 1.5 mmol/L,cHCO3-P.c 20.9 mmol/L(↓)。
WBC 22.57×109/L(↑),NEU% 92.7%,PCT 0.130 ng/ml(↑),ESR 82 mm/h,CRP 183 mg/L。
肝功能:ALT 66.7 U/L(↑),AST 96.7 U/L(↑)。
随机血糖最高25 mmol/L,β-羟丁酸1.23 mmol/L,尿酮阳性,HbA1c 5.9%。
BNP 973.1 pg/ml。
床旁心电图示快速房颤。
美罗培南1 g ivgtt q8h抗感染。
甲强龙40 mg q12h抗炎。
细辛脑化痰、还原性谷胱甘肽护肝、奥美拉唑护胃、低分子肝素抗凝、降糖等对症处理。
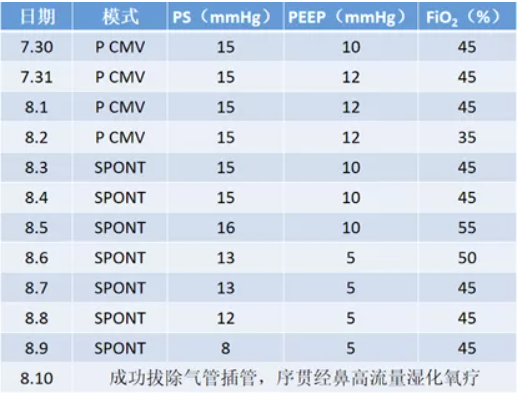
有创呼吸机辅助呼吸:7月28日,SPONT模式,PS 23 mmHg,FiO2 70%,SpO2 92%。7月29日下午,CMV模式,VT 420 ml,PEEP 10 cmH2O,FiO2 100%,SpO2 74%。7月29日晚上,采取俯卧位,CMV模式,VT 420 ml,PEEP 10 cmH2O,FiO2 100%,PaO2 44 mmHg,SpO2 83%。
7月28-29日,患者肺部病变明显加重(图9)。
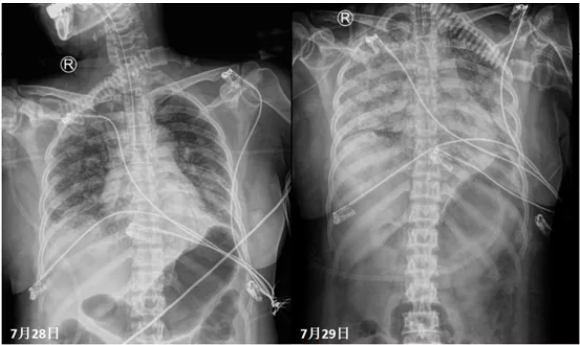
讨论二:肺部病变加重的原因? |
专家讨论
这一阶段是在激素减量过程中,作为免疫缺陷宿主发生的重症肺炎,核心问题是脓毒症、ARDS及MODS。第一,在呼吸支持治疗阶段,氧合恶化且难以维持,在这种情况下,除外感染中毒和结缔组织疾病导致的心肌损害,其中涉及血流动力学的监测和心脏功能的评估,所以后续的俯卧位、镇痛镇静、肌松等均可以尝试。但是如果氧合指数明显下降(<50 mmHg),应予以考虑行ECMO。第二,从经验性抗感染治疗方面来看,将碳青霉烯类作为起始的抗革兰氏阴性菌的治疗药物是可行的,但剂量可能不足,对于脓毒症来说仍值得商榷。需要区分感染控制和器官功能,包括循环稳定性和呼吸衰竭。感染可以得到控制,在有效的高级生命支持管理方面,如果存在疾病进展或缓解延迟,可以考虑补救性替代治疗措施。第三,无论患者有无激素治疗背景,评估激素对免疫功能的损害及对血糖的影响等,有助于治疗原发病。第四,除了ARDS、MODS外,仍存在肺水肿的因素,较为突出的问题是血糖升高和氧合指数降低。结合患者HbA1c指标分析,患者应为应激性血糖异常,考虑糖尿病的可能,与糖皮质激素继发的血糖升高有关。
这一阶段的“查因”与治疗同样重要。首先,我们需要尽快明确此时是原发基础疾病的进展还是合并了新的感染。其次,需要明确是否有肺水增多的情况存在,导致其氧合极度低下。患者的低血压可能与插管后的镇静有关,而非感染性休克。再次,患者WBC、血糖、CRP水平均升高,虽然长期使用激素(50余天)导致免疫低下可能引起病原微生物感染,我们确实需要考虑,但患者病情进展太快,仅1天的时间就进展为“白肺”,我个人认为可能存在肺水增多的情况。
患者7月28日行有创呼吸机辅助呼吸的PS为23 mmHg,肺部病变加重,有无可能与跨肺压增高或机械通气有关。
这一阶段患者主要存在两个问题,一是严重的呼吸衰竭,二是低血压。导致呼吸衰竭的原因首要因素考虑感染,关键需要明确导致感染的病原学。此阶段患者免疫功能低下,激素使用接近2个月,结合影像学和气管镜,未见明显的化脓性改变。此时病情加重不应将细菌作为重点考虑,而应关注PCP和CMV感染。其次,导致呼吸衰竭的原因不能除外原发病加重,虽然初期使用了激素,但如果考虑ICU患者的COP,激素使用剂量往往大于常规,所以激素剂量要加大。另外,需要尽快做气管镜,明确病原学。对于患者低血压情况,我个人不认为是感染性休克,虽然感染可能在其中发挥了一定作用。我认为低血容量和呼吸机参数调节可能是低血压的诱因。机械通气后,PEEP较高,潮气量450 ml,对于此阶段的患者来说,气道压偏大,加上采取了镇静镇痛措施,可能使患者血压下降。采取俯卧位后患者氧合改善也不理想,所以肺的可复张性较小,PEEP意义不大。所以此时对于该患者的支持手段应为ECMO,患者原发病应是可治的,且无ECMO禁忌证,可以尽快给予ECMO支持。
病变加重原因
3次血培养均阴性。
血NGS:细菌、真菌、寄生虫、结核、NTM、支原体/衣原体均阴性。DNA病毒提示人类疱疹病毒5型(CMV),序列数8。
纤支镜:右中叶可见少许血性分泌物,于右下叶行肺泡灌洗。
肺泡灌洗液:涂片镜检、革兰染色、GM试验、细菌+真菌培养均阴性。
肺泡灌洗液NGS:产气克雷伯菌(序列数7),粪肠球菌(序列数5),耶氏肺孢子菌(序列数5),新生隐球菌(序列数2),CMV(序列数14),人疱疹病毒7型(序列数4)(图10)。
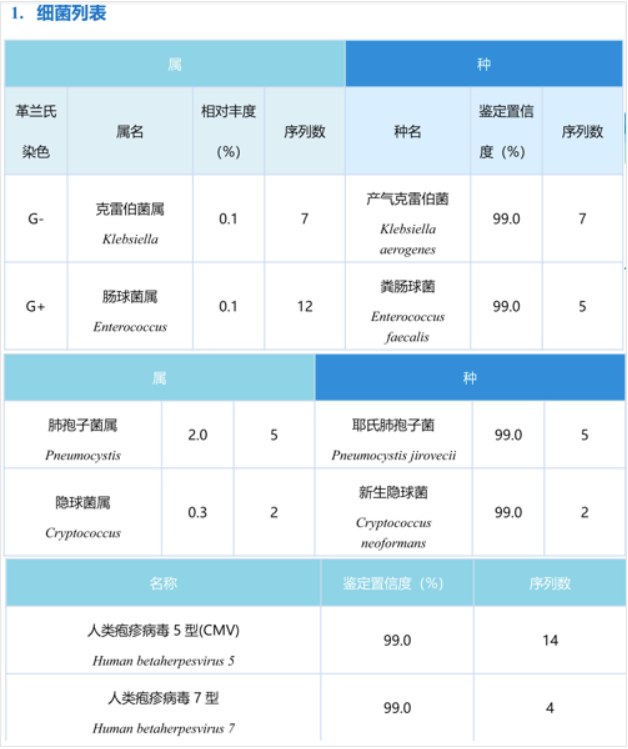

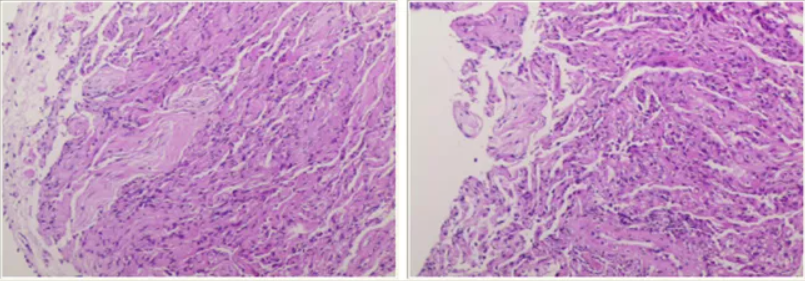
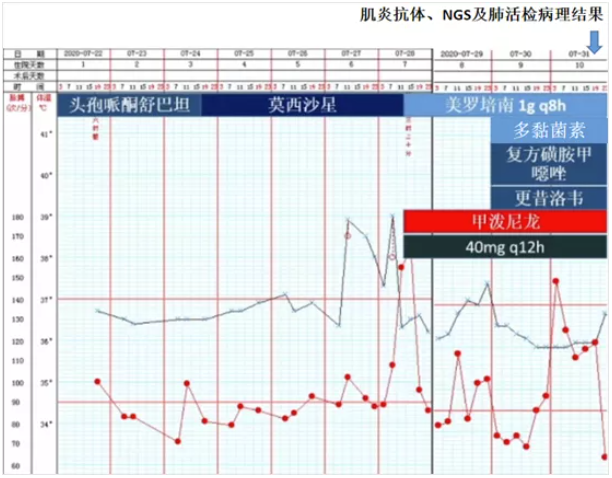
专家讨论
根据NGS结果提示产气克雷伯菌、粪肠球菌、耶氏肺孢子菌、新生隐球菌、CMV、人疱疹病毒7型。某种意义上来讲,病毒感染会导致细菌感染的快速恶化。从临床进展和特征分析,感染的程度与器官功能有相关性。就这例患者而言,肺水的管理可能是重点,呼吸功能在ECMO支持后获得改善,关键是抗感染疗效。基于目前的方案,基本已经覆盖了检出的病原菌,但主要线索我认为是肠杆菌+CMV,其他的不作为主要考虑。目前的治疗方案我认为是合理的,对于重症患者,尽量覆盖可能的病原菌,为抢救生命赢得时间。
NGS的作用取决于各中心微生物实验室的能力。第一,这例患者具备获得PCP的高危风险。如果其他条件不存在,我也会考虑长期使用激素患者、气管镜下无明显感染表现、胸部影像学改变,加上NGS回报,可能是PCP。这例患者六胺银染色阴性,并不支持PCP的诊断,如果拿到NGS结果后,可以通过微生物实验室验证这一结果的准确性,考虑患者存在高危风险,复方磺胺甲噁唑还应使用。第二,在长期使用激素的情况下,CMV的NGS结果的临床意义有待商榷,我个人可能不考虑对其进行干预,或者采取相对保守策略。第三,在获取上述NGS后,抗生素治疗方面我可能会做一些减法。
NGS回报CMV拷贝数较低,所以预防性使用更昔洛韦我认为是可以的。我们临床会遇到骨髓移植免疫抑制患者,CMV拷贝数>100,NGS的意义可能更大。另外,其耶氏肺孢子菌的拷贝数也不高,需要结合当地医院微生物实验室结果进行综合判断。但对于免疫抑制患者,给予复方磺胺甲噁唑和更昔洛韦不论预防还是治疗都是可行的。
治疗方案
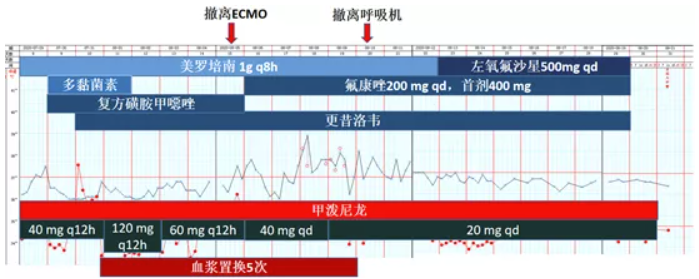
根据8月1日回报的肌炎抗体、NGS及肺活检病理结果,调整治疗方案:多黏菌素75万单位静滴q12h(7月30日至8月1日),之后停药。美罗培南1 g静滴q8h(7月28日至8月12日)。复方磺胺甲噁唑片3片口服q6h(7月30-31日),2片口服qd(8月1-5日)。更昔洛韦125 mg静滴q12h(7月31日至8月2日),125 mg静滴qd(8月3-19日)。甲泼尼龙:40 mg q12h(7月29-31日),120 mg q12h(8月1-2日),60 mg bid(8月3-5日)(图14)。
血浆置换术。
维持每天液体负平衡。
营养支持,护胃,护肝,护肾,抗凝,调节肠道菌群。
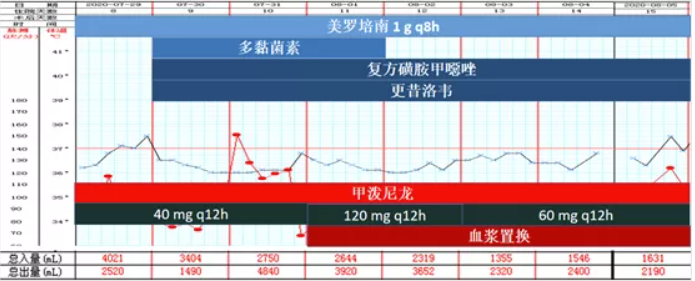
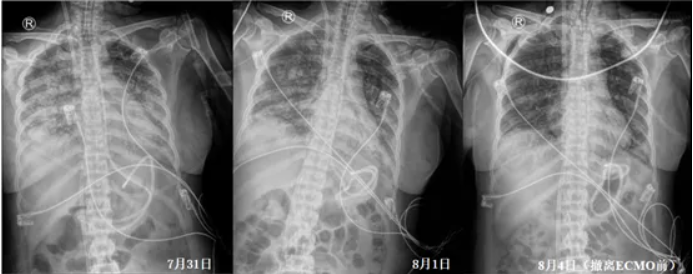
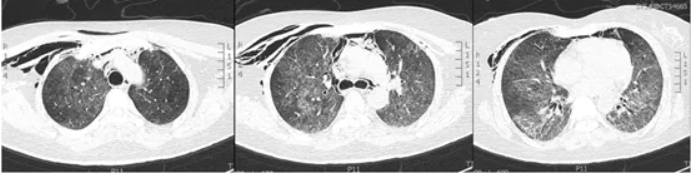
图17 患者胸部CT(撤离ECMO后)
专家讨论
针对这例免疫抑制患者,我可能会考虑先撤呼吸机再撤ECMO。气压伤很难避免,这类患者即使不采取机械通气,也可能出现气压伤。
患者经过治疗后,氧合很快改善,说明激素在其中确实发挥了作用。在原发病方面,除了考虑感染外,非感性性疾病在其中也占了很大的比重。这例患者出现气压伤有几方面原因,①ECMO流量不足,没有充分发挥辅助作用,如果ECMO流量达到4 L/min,那么其对患者的呼吸支持就非常强,患者自身负荷减轻,有利于肺休息。②PEEP相对过高。该患者已经出现肺纤维化,这种情况对PEEP的反应欠佳,包括机化本身对PEEP的反应也较差,机化是终末气道和肺泡腔的肉芽样填充,给予PEEP无效,只能依靠自身修复和吸收,所以这例患者的PEEP设置为6~8 mmHg即可。③可能与患者后期病变有关。机化性肺炎后期也会出现肺纤维化,而且这例患者早期胸部CT已经提示出现肺纤维化,如果合并PCP,更容易出现皮下气肿。如果发现了纵隔气肿,ECMO尽量晚撤。因为ECMO除了改善氧合和通气外,还能让肺得到充分的休息。而且这例患者ECMO上机不足1周,维持效果也很好,这时可以先拔出气管插管,撤离呼吸机,让患者咳痰,避免出现VAP。
后续治疗方案
将美罗培南改为左氧氟沙星500 mg静滴qd(8月13-19日)。痰培养发现白念珠菌,故加用氟康唑200 mg静滴qd(8月6-19日)。患者出现肾功能损害,故停用复方磺胺甲噁唑。更昔洛韦继续使用125 mg静滴qd(8月3-19日)。甲泼尼龙40 mg qd(8月6-8日),20 mg qd(8月9日开始)(图19)。
血浆置换术5次。
营养支持,护胃,护肝,护肾,抗凝,调节肠道菌群。
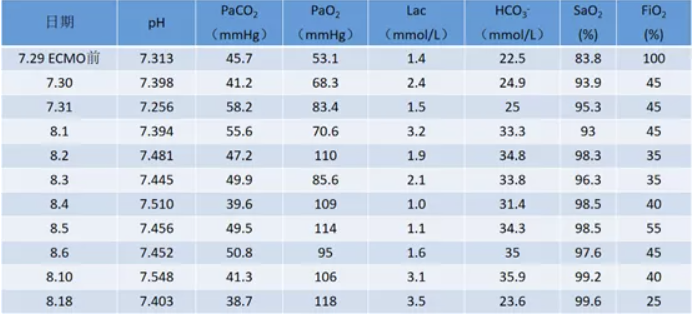
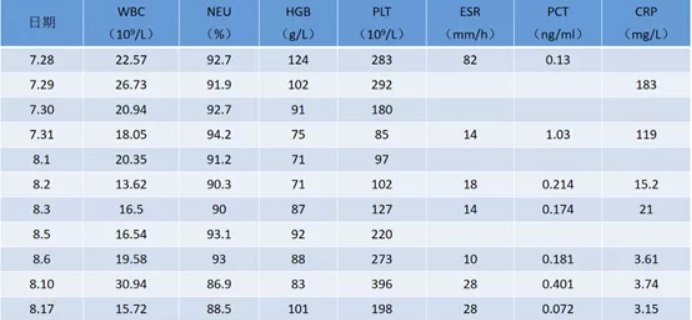
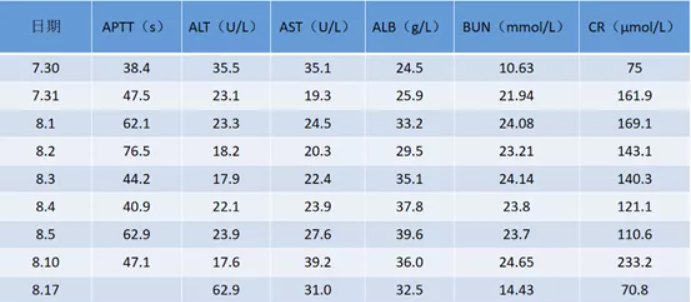
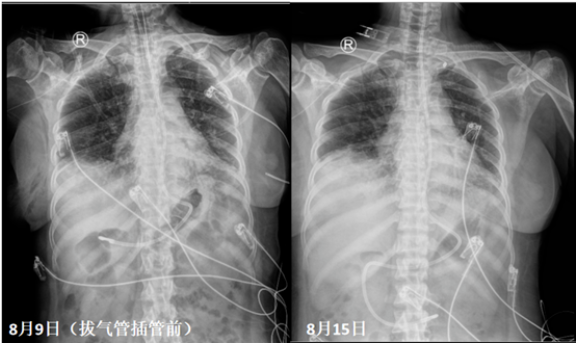
转归
8月20日,患者出院。
出院后继续予口服甲泼尼龙20 mg qd治疗。
9月7日,随访复查胸部CT:肺部渗出灶和纤维条缩影明显吸收好转,纵隔气肿消失(图24)。
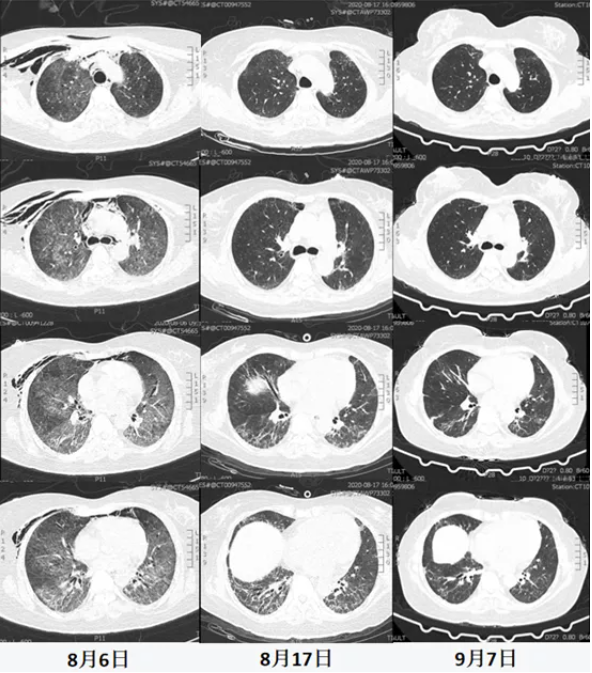
总结
|
 后可发表评论
后可发表评论




友情链接
联系我们
 公众号
公众号
 客服微信
客服微信