登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
指导老师:秦浩(海军军医大学第一附属医院呼吸与危重症医学科)
【摘要】前期内容我们探讨了重症超声对于心脏功能的评价,循环系统除开心脏,心脏直连的大血管、外周脏器的灌注(尤其是肾脏、肺的灌注)、心肺交互也需要我们关注。本文将从大血管、血流动力学和循环、血管外肺水和心肺交互等的超声评估来展开讨论,从而让我们更好地应用重症超声这个手段来对重症患者进行评估和治疗。
1
重症超声对大血管的评估
针对心脏的最核心的大血管超声评估(经胸心脏超声)而言,涉及主动脉、肺动脉、下腔静脉(IVC)和上腔静脉、肺静脉的评估。
我们在胸骨旁长轴切面或胸骨上窝切面评估主动脉。在胸骨旁长轴切面的示意如图1所示,在胸骨上窝切面如图2所示。
图2 胸骨上窝切面主动脉示意图
图3 胸骨旁短轴肺动脉切面示意图
图4 剑突下四腔心下腔静脉切面
2
重症超声对循环的评估
2.1 重症超声对体循环前负荷的评价(静态指标和动态指标)
图5 下腔静脉的测量
2.2 重症超声对体循环心脏收缩功能的评价(整体和局部)
左室短轴缩短分数(FS):24%~36%;
面积缩短率(LV-FAC)38%~60%;
左室射血分数(LV-EF):>60%;
图8 左心室分节段心肌运动斑点追踪示意图
图9 左心室分节段心肌运动斑点追踪二维成像应变测量汇总示意图(牛眼图)
2.3 体循环后负荷的评价
SVRI=80×(MAP-CVP)×BAS/CO
2.4 重症超声对肺循环的评估
图11 舒张末LV与RV面积对比测量示意图(左边比值正常,右边比值异常)
图12 肺血管阻力的计算参考示意图
3
心肺交互和容量反应性
对于血流动力学和循环的评价,我们绕不开的话题之一就是心肺交互作用。关于心肺相互作用的关系,我们整理了图14供参考。
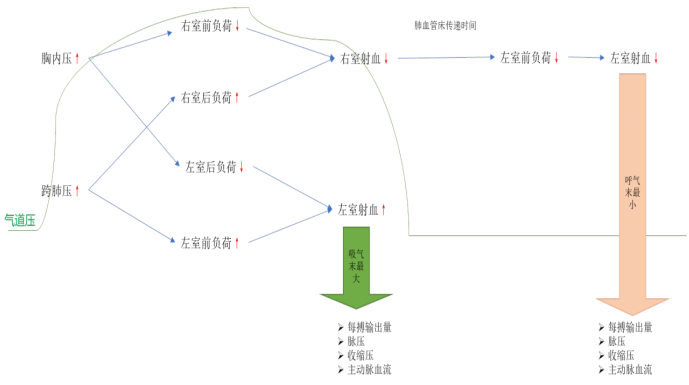 图14 心肺交互关系图
图14 心肺交互关系图图15 主动脉峰流速变异率测量
图17 液体管理优化流程
4
血流动力学的评价
超声对血流动力学的整体评价,现阶段推荐的还是以CCUE方案为核心的FREE流程,前文已经分享了血流动力学的六步法,现将超声的FREE方案呈现如下(图18),供参考。
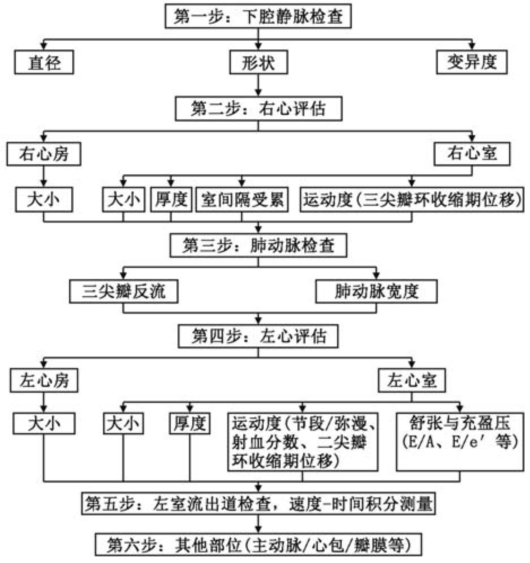
图18 FREE流程为核心的血流动力学评价超声系统
5
总结
超声作为ICU床边常用的手段之一,随着研究的不断深入,其临床上应用层面已经从单纯的脏器评估的层面,升级为系统层面的支持、指导和治疗方向的把控。“重症超声”专题的3篇文章分别从重症超声和机械通气的参数设置精准化、重症超声和心脏功能的评价、超声和循环功能的评价与心肺交互三个层面,对重症超声在ICU中的应用予以阐述。希望我们能将这一技术更多、更好地用于临床,为临床诊疗行提供有效帮助。
参考文献
[1] Rudski L G, Lai W W, Afilalo J, et al. Guidelines for the Echocardiographic Assessment of the Right Heart in Adults: A Report from the American Society of Echocardiography Endorsed by the European Association of Echocardiography, a registered branch of the European Society of Cardiology, and the Canadian Society of Echocardiography[J]. J Am Soc Echocardiogr, 2010, 23(7):685-713; quiz 786-8.
[2] Mitchell C, Rahko P S, Blauwet L A, et al. Guidelines for Performing a Comprehensive Transthoracic Echocardiographic Examination in Adults: Recommendations from the American Society of Echocardiography. Journal of the American Society of Echocardiography[J]. J Am Soc Echocardiogr, 2019, 32(1):1-64.
[3] Hunt J, Anas N. Monitoring Cardiopulmonary Interactions: Where Are We Going?[J]. Pediatr Crit Care Med, 2014, 15(1):84-85.
[4] Kasprzak J D, Huttin O, Wierzbowska-Drabik K, et al. Imaging the Right Heart-Pulmonary Circulation Unit: The Role of Ultrasound[J]. Heart Fail Clin, 2018, 14(3):361-376.
[5] Reant P, Metras A, Detaille D, et al. Impact of Afterload Increase on Left Ventricular Myocardial Deformation Indices[J]. J Am Soc Echocardiogr, 2016, 29(12):1217-1228.
[6] De Backer D, Aissaoui N, Cecconi M, et al. How can assessing hemodynamics help to assess volume status?[J]. Intensive Care Med, 2022, 48(10):1482-1494.
[7] 尹万红, 王小亭, 刘大为, 等. 重症超声临床应用技术规范[J]. 中华内科杂志, 2018, 57(6):397-417.
作者介绍
潘宾海
南京大学医学院附属金陵医院呼吸与危重症医学科RICU呼吸治疗师
毕业于四川大学华西临床医学院呼吸治疗专业
主要工作研究领域:呼吸与危重症患者的呼吸支持、气道管理、床边支气管镜诊治、重症超声的应用等
指导老师
秦 浩
海军军医大学第一附属医院呼吸与危重症医学科主管呼吸治疗师
专业方向为机械通气、危重症监护及呼吸介入
中国医学装备协会呼吸病学装备技术专业委员会委员
中国康复医学会呼吸康复专委会第二届委员会呼吸治疗学组委员
中国医师协会内镜医师培训学院呼吸内镜资深讲师
上海市医学会呼吸病学专科分会呼吸治疗学组(筹)委员兼秘书
上海呼吸治疗联盟核心成员
长海医院微创精品课程导师
发表SCI及核心期刊8篇
参与制定专家共识2项,参编参译多部著作,获实用新型专利3项
参与国家级课题1项,省部级课题3项,校级课题2项
 后可发表评论
后可发表评论




友情链接
联系我们
 公众号
公众号
 客服微信
客服微信