登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
作者:崔晓阳
单位:国家呼吸医学中心 中国医学科学院呼吸病学研究院 中日医院呼吸中心
目前已知呼吸道合胞病毒(RSV)是婴幼儿下呼吸道感染的重要原因,可导致住院和死亡。然而,它对成人的影响直到最近几年才被认识到。随着病原微生物检测手段的进步,越来越多的研究发现,RSV对于成人尤其是老年人和有基础疾病的人群,也是非常重要的一类病原体。

COVID-19对RSV流行也产生了重大影响。COVID-19流行期间,由于口罩、手卫生、旅行限制以及社交距离等因素的控制,使RSV的检出率大幅下降。意大利一项研究显示,RSV检出率由COVID-19流行前的5%降至0.14%(2017—2021年)。随着疫情控制政策的放松以及易感人群的增加,2022年冬季至2023年冬季,在RSV流行大幅下降的2年后,RSV在多个国家大面积爆发。


RSV的传播风险因人群及管控措施不同而不同,在新生儿病房为28.5%,骨髓移植病房,为30%,其他成人患者为30%~32%。并且,RSV的传播具有基因易感性,与异卵双胞胎相比,同卵双胞胎发生重症RSV感染的一致率明显增高(一致率0.66 vs. 0.53,P=0.02),提示遗传因素在重症RSV感染中的作用。

RSV的易感人群包括:婴幼儿(5岁以下)、老年(60岁以上);基础疾病多(慢性肺部疾病占35.6%,心血管疾病占51%);免疫抑制(肺和造血干细胞移植、肿瘤、免疫抑制治疗)患者。RSV的感染贯穿人的一生,但疾病负担最重还是在首尾两端,即新生儿及幼童和65岁以上老年人。

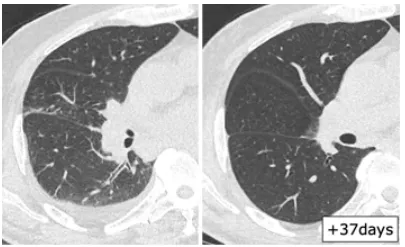
图1 63岁T淋巴细胞瘤患者感染RSV的影像学表现
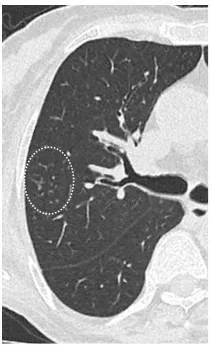
图2 75岁T淋巴细胞瘤患者感染RSV的影像学表现
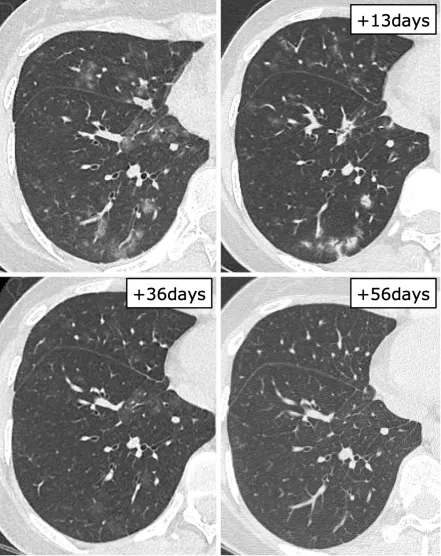
图3 23岁急性粒细胞白血病患者感染RSV的影像学表现
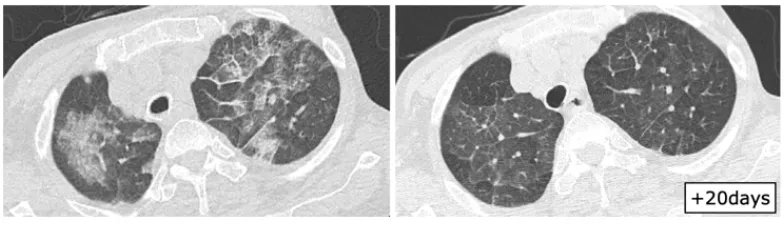
图4 78岁慢粒患者患者感染RSV的影像学表现
图源:Intern Med. 2020;59(2):247-252.

1996年1月至2009年5月在德克萨斯大学MD Anderson癌症中心进行了一项大型回顾性单中心研究,研究对象为所有实验室证实RSV感染的异基因造血干细胞移植受者。研究对237例RSV上呼吸道感染患者进行危险因素分析,制定免疫缺陷评分(immunodeficiency scoring index,ISI)分级系统。通过对患者粒细胞和淋巴细胞计数、年龄、骨髓移植情况、有无移植物抗宿主病、有无使用激素等因素进行评估,然后对患者进行危险分层。分层后发现,ISI评分风险越高,RSV由上呼吸道感染进展至下呼吸道感染的风险越高,死亡风险也越高。予以抗病毒治疗后,任何风险组进展为下呼吸道感染以及死亡的比例都有所下降,且风险越高的患者,抗病毒治疗获益越大。


目前也有很多新的抗病毒药物处于研发阶段,也包括我们国家的AK-0529Ⅲ期临床研究。除了抗病毒药物非特异性免疫球蛋白(Asceniv®,ADMA Biologics)由于含有非特异性的RSV抗体,也可以对患者起到一定的免疫支持作用。

RSV是免疫低下、有基础疾病患者及老年人的常见病原体,其发病率及病死率与流感相当。分子诊断的进展可以实现RSV感染的迅速诊断,RSV疫苗和单克隆抗体的上市为高危人群提供了更好的保护。RSV抗病毒药物仍然有限,是目前的研究重点,对于高危人群RSV感染,利巴韦林仍然占有一定的地位。
参考文献
作者介绍
主治医师,医学博士,中日友好医院呼吸与危重症医学科,毕业于四川大学华西临床医学院,完成PCCM专科培训,从事呼吸危重症相关临床及科研工作,主要研究方向为ECMO相关呼吸支持手段,以第一作者在相关领域发表SCI论文多篇。
 后可发表评论
后可发表评论




友情链接
联系我们
 公众号
公众号
 客服微信
客服微信