登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
病例1. 当肾移植患者遭遇“白肺”
单位:国家呼吸医学中心 中日友好医院呼吸与危重症医学科
病情介绍
一般情况
患者,男性,62岁,体重55 kg,2022年12月19日入院。主诉:反复发热、咳嗽、咳痰、呼吸困难12天,加重4天。
12天前无明显诱因开始出现反复发热,Tmax 38.5℃,无畏寒、寒战,伴全身酸痛,伴咳嗽、咳少量黄白痰,有痰不易咳出,伴呼吸困难(患者曾于15天前查新冠核酸阳性,当时无症状),自服连花清瘟胶囊2粒,效果不佳,曾有2天体温正常,随后再次出现发热,体温波动于37~38℃。
4天前上述症状加重,咳嗽明显,咳少量黄白痰,自觉有痰不易咳出,呼吸困难较前加重,稍事活动即出现呼吸困难。
1天前于当地医院查血常规示WBC 7×109/L,LYM 0.11×109/L(↓),CRP 133.9 mg/L(↑);肝肾功能检查示BUN 11.64 mmol/L(↑),Cr 123.2 μmol/L(↑),K 5.55 mmol/L,Na 127.9 mmol/L(↓);胸部CT示双肺多发斑片状磨玻璃影。
为进一步诊治前来我院,急诊以“重症肺炎”收入我科。患者自起病以来,精神、睡眠尚可,饮食不佳,大小便正常,体重较前无明显变化。
高血压病史30年,血压最高200/140 mmHg,目前口服硝苯地平控释片30 mg每日一次,血压控制可。糖尿病病史20年,目前应用门冬胰岛素16 IU三餐前、甘精胰岛素10 IU睡前皮下注射,血糖控制可。
8年前因“肾囊肿”行左肾切除术,后患泌尿系感染(具体不详),3年前因肾功能不全开始行透析治疗,5月前(2022年7月21日)于我院行同种异体肾移植术,术后规律口服他克莫司、醋酸泼尼松龙、麦考酚钠肠溶片抗排异治疗及磺胺2片预防感染、碳酸氢钠0.5 g每日三次、碳酸钙片0.75 g每日三次+骨化三醇0.25 μg每日一次补钙、酒石酸美托洛尔25 mg每日一次+盐酸特拉唑嗪4 mg每日一次降压、非布司他20 mg每日一次降尿酸、叶酸5 mg每日两次、罗沙司他100 mg每周三次。
2021年接种3针新冠疫苗(具体不详)。
否认冠心病、脑血管疾病、精神疾病病史,否认肝炎、结核病史,否认外伤、输血史;否认食物、药物过敏史。
出生并久居于河北省保定市定州市,无疫水、疫区接触史,无牧区、矿山、高氟、低碘区居住史,无特殊化学物质、放射性物质、有毒物质接触史,无吸毒史,吸烟40年,20~30支/日,未戒烟,否认饮酒史,无冶游史。适龄婚育,育有1子1女,配偶及子女体健。父母已故,死因不详,否认家族性遗传病史。
T 36.2℃,P 100次/min,RR 26次/min,BP 124/78 mmHg。发育正常,营养良好,神志清楚,喘息貌,口唇无发绀;双肺呼吸音清,未及干/湿啰音,无胸膜摩擦音;心率100次/min,心音有力,律齐,各瓣膜区未及杂音;下腹部可见手术瘢痕,愈合良好,腹软,无压痛、反跳痛,未触及包块;双下肢无水肿。
重症社区获得性肺炎(新型冠状病毒感染,重型),Ⅰ型呼吸衰竭;
慢性肾功能不全,异体肾移植状态,肾性贫血;
左肾切除术后;
高血压3级,极高危组;
2型糖尿病;
血常规:WBC 8.04×109/L,NEU 7.47×109/L,LYM 0.12×109/L,HGB 98 g/L,PLT 249×109/L。
PCT 0.19 ng/ml,CRP 126.04 mg/L,铁蛋白1192.6 ng/ml。
淋巴细胞亚群:CD4+ T淋巴细胞70 cells/ul。
免疫球蛋白+补体:IgM 38 mg/dl,余项正常。
血气分析(HFNC 40 L/min,FiO2 0.7):pH 7.36,PaCO2 29.5 mmHg,PaO2 74 mmHg,HCO3- 27.5 mmol/L,BE 3.8 mmol/L,Lac 3.0 mmol/L,P/F 106 mmHg。
心梗四项:cTnT 0.023 ng/ml,NT-proBNP 624 pg/ml。
床旁超声心动图:室间隔增厚,主动脉瓣硬化。
肝肾功能:ALT 16 IU/L,AST 21 IU/L,ALB 35.9 g/L,Urea 9.81 mmol/L,CR 126.6 μmol/L,K 4.6 mmol/L,Na 131 mmol/L。
FK506 24 ng/ml。
凝血六项:PT 14.3 s,APTT 39.7 s,Fib 6.3 g/L,D-Dimer 2.03 mg/L。
12月20日胸部CT可见双肺弥漫分布的磨玻璃影,以胸膜下、双下肺为著,双下肺有实变表现。
治疗经过
IVIG 10 g qd静点。
脏器功能支持
营养:自主进食,门冬+甘精胰岛素控制血糖。
其他辅助治疗
补钙:碳酸钙片0.75 g bid、骨化三醇0.25 μg qn。
辅助检查-病原学
D1-D8病情及治疗
脏器功能
治疗
IVIG 10 g qd静点(12月19-26日)。
继续原治疗方案(呼吸支持、维持循环、抗凝、营养)。
乳果糖通便。
病情变化
12月27日(D8)复查胸部CT:双肺病变范围较前稍有扩大,实变增加,以双下肺为著,尤其是右下肺。
辅助检查—病原学
D9-D17病情及治疗
插管后早期患者体温未降,感染指标升高,将哌拉西林他唑巴坦调整为亚胺培南西司他丁,LYM回升后再次降低,CRP、铁蛋白升高。
辅助检查-病原学
BALF病原学:细菌培养示CRAB(仅对替加环素、多黏菌素敏感)。
影像学
2023年1月3日复查胸部CT:双肺弥漫磨玻璃影密度有所减低,出现明显的气压伤,包括气胸、皮下/纵隔气肿。
脏器功能
治疗
(1)寻求抗感染、抗炎与抗排异的平衡
抗感染:结合病原学检查结果,调整抗感染方案,亚胺培南西司他丁(2022年12月27日至2023年1月4日),替加环素(1.1-)+舒巴坦(2023年1月4日-),伏立康唑片,磺胺。
抗炎:考虑患者出现VAP,将激素减量,甲泼尼龙80 mg qd静点(2022年12月29-31日),逐渐降至40 mg qd(2023年1月1-3日)、20 mg qd(1月4日),考虑IL-6和铁蛋白升高,遂给予托珠单抗一次(1月3日)。
(2)脏器功能支持
呼吸支持:气管插管→气管切开,PEEP 10 cmH2O,FiO2 0.5~0.6,俯卧位。
循环:无血管活性药,监测血压、心率、出入量。
抗凝:依诺肝素钠4000 IU qn皮下注射预防性抗凝。
(3)其他辅助治疗
祛痰、抑酸、补钙、通便同前。
纠正低蛋白血症:白蛋白20 g qd静点。
病情及治疗概括
患者2022年12月19日入院,当时WBC和体温均正常,CRP、IL-6、铁蛋白明显升高,P/F 100 mmHg,及时完善气管镜检查,发现曲霉,哌拉西林他唑巴坦+伏立康唑抗感染治疗。抗炎治疗使用甲强龙40 mg qd,连用5天。治疗后炎症指标下降,但氧合恶化,影像学进展,12月29日气管插管,镜下相对干净,加强激素治疗(80 mg qd,连用3天)。后续患者感染指标明显升高,BALF培养CRAB,调整抗感染治疗为替加环素+舒巴坦,继续使用伏立康唑和磺胺。调整治疗后,影像学仍有进展,并且出现了气压伤,铁蛋白较前回升,在抗感染保驾和每日气管镜吸痰的情况下使用托珠单抗一次,患者体温逐渐恢复正常,WBC、PCT、CRP明显下降,氧合指数缓慢上升。
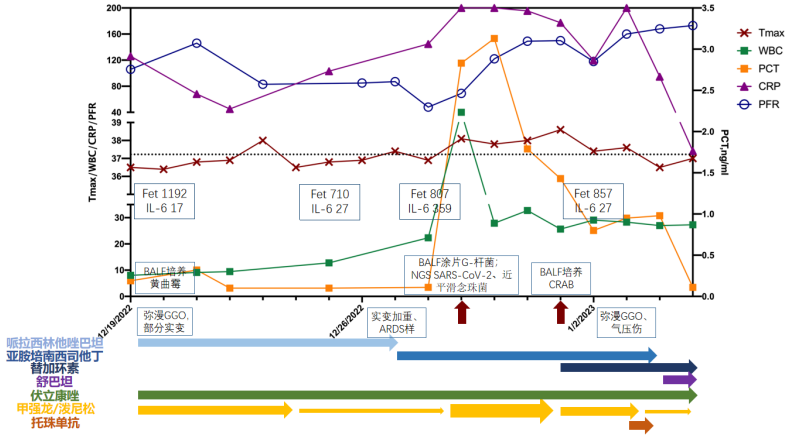
(3)呼吸支持策略:本例患者影像学可见重力依赖区的病变更为严重,患者能否从早期清醒俯卧位中获益?能否真正改善预后?是否早期气管插管、气管切开会对改善预后有所帮助?如何把握此类患者ECMO的应用指征?
病例2. 高龄、危重型新冠肺炎合并MRSA—如何把握抗炎与抗感染之间的平衡
作者:黄琳娜
单位:国家呼吸医学中心 中日友好医院呼吸与危重症医学科
病情介绍
2周前(12月8日)无明显诱因间断出现反酸、呕吐,呕吐物为少量胃内容物,无呕血,自测体温37℃,口服藿香正气水稍缓解,12月12日自测新冠抗原(+),伴发热,Tmax 38℃,无咽痛、咳嗽、咳痰、呼吸困难等,间断口服连花清瘟、小柴胡颗粒、芬必得,期间可正常日常活动。
3天前(12月19日)出现呼吸困难、烦躁伴双下肢水肿,无法平卧,需坐位入睡,自测SpO2(未吸氧)90%~92%,症状持续不缓解,遂于12月21日至我院急诊,予面罩吸氧15 L/min,莫西沙星0.4 g+奥司他韦75 mg bid,化痰、利尿等对症治疗。SpO2(未吸氧)85%。血气分析(FiO2 0.21):pH 7.39,PaCO2 23 mmHg,PaO2 68 mmHg,PFR 324 mmHg,BE -9.2 mmol/L,Lac 1.3 mmol/L。血常规:WBC 7.51×109/L,NEU 6.53×109/L(↑),LYM 0.47×109/L(↓),Hb 117 g/L(↓),CRP 83.09 mg/L(↑)(<10)。肝肾功能:ALT 36 IU/L,AST 51 IU/L(↑),K 5.0 mmol/L,Na 125.9 mmol/L(↓),Cr 299.5 μmol/L(↑)。心梗四项:Myo 943.60 ng/ml(↑),CK-MB 7.65 ng/ml(↑),cTnT 0.086 ng/ml(↑)(<0.014),Nt-proBNP 10354 pg/ml(↑)(<125)。
12月21日胸部CT可见双肺散在磨玻璃斑片影,部分沿支气管血管束分布。
12月22日复查上述检查。血气分析(面罩吸氧15 L/min):pH 7.25,PaCO2 27 mmHg,PaO2 54 mmHg,BE -13.9 mmol/L,Lac 5.1 mmol/L。血常规:WBC 6.51×109/L,NEU 5.45×109/L,LYM 0.66×109/L(↓),CRP 100.23 mg/L(↑)。肝肾功能:ALT 30 IU/L,AST 56 IU/L(↑),Cr 329.1 μmol/L(↑),Na 126.5 mmol/L(↓)。心梗四项:Myo 1111.00 ng/ml(↑),CK-MB 11.74 ng/ml(↑),cTnT 0.080 ng/ml(↑)(<0.014),Nt-proBNP 11990 pg/ml(↑)(<125)。
现为进一步诊治收入我科。患者自发病以来,精神、食欲、睡眠差,小便量较前减少,体重变化不详。
高血压30余年,硝苯地平控释片30 mg qd+培哚普利4 mg qd,血压控制于130~140/60~80 mmHg。糖尿病30余年,利格列汀5 mg qd+瑞格列奈1 mg早餐前/3 mg午餐前/1 mg晚餐前,门冬胰岛素18 IU午餐前。冠心病10余年,2012年LCX和LAD各置入支架1枚,2018年行支架内溶栓及球囊扩张术,房颤病史3余年,长期规律服用艾多沙班。慢性肾脏病、肾性贫血、重度骨质疏松4年,服用开同、尿毒清、铁剂、碳酸钙、骨化三醇。高尿酸血症7年,非布司他40 mg qd。20余年前曾因白内障行“晶体置换术”。吸烟20余年,3~4支/日,戒烟30余年,无饮酒史。未接种新冠疫苗。适龄婚育,育有2女1子,配偶高血压、高血脂、糖尿病、脑梗、老年痴呆,儿子糖尿病。父母已故,父亲高血压。
T 36.7℃,HR 120次/min,RR 42次/min,BP 154/46 mmHg。SpO2(HFNC FiO2 1.0+储氧面罩15 L/mim)85%~90%。端坐位,痛苦面容,口唇发绀,颈静脉无怒张;双肺可闻及散在干/湿啰音,无胸膜摩擦音;心尖搏动位置正常,心界无扩大;心率120次/min,心音有力,律齐,各瓣膜听诊区未闻及杂音,无心包摩擦音;腹软,无压痛、反跳痛,肝脾未触及;双下肢未见水肿。
老年男性,急性病程;
既往高血压、冠心病、房颤、糖尿病病史;吸烟史;未接种新冠疫苗;
反复呕吐伴发热,并逐渐出现进行性加重的呼吸困难,抗细菌及抗流感病毒治疗效果不佳;入ICU至起病时间为15天;
呼吸频率及心率明显增快,伴SpO2明显下降,储氧面罩吸氧无法维持;
WBC不高,LYM下降,CRP明显增高;cTnT、NT-proBNP明显增高;Scr升高;代谢性酸中毒、乳酸增高;
CT提示双肺散在磨玻璃斑片影,部分沿支气管血管束分布。
辅助检查及诊疗经过
新冠抗原(12月12日):(+)。
新冠核酸(鼻咽拭子,12月23日):(+),CT值22。
新冠核酸(鼻咽拭子,12月26日):(+),CT值28。
新冠核酸(鼻咽拭子,12月29日):(+),CT值31。
患者入ICU时距起病已15天,不能除外合并感染,加之当时患者入院最初的PCT明显增高,所以在入院最初5天,主要以哌拉西林他唑巴坦经验性抗感染治疗为主,并且加用地塞米松6 mg抗炎。
12月22日血G/GM试验(-);血EB/CMV核酸定量(-);外周血培养(双上肢)阴性。12月26日气管镜黏膜充血水肿明显,各叶段可吸出中等量稀薄淡血性分泌物,各叶段少量白色黏痰,以右肺著,于右肺中叶予支气管肺泡灌洗,回收淡血性稀薄分泌物。12月23日BALF ETA病原学:细菌涂片/培养(-);真菌涂片/培养(-)。12月26日BALF病原学:涂片G+球菌成堆中等量;细菌培养为MRSA;真菌涂片(-);真菌培养:白念珠菌;BALF-GM(-);BALF NGS:金葡菌(序列数13177),屎肠球菌(序列数470),洋葱伯克霍尔德菌(序列数390)。
动态监测患者的炎症指标,CRP>75 mg/L,铁蛋白>1000 ng/ml,处于持续偏高状态,并且在最初经验抗感染治疗过程中,患者PCT呈逐渐下降趋势。2022年12月27日复查胸部CT:在原有病变基础上出现了动态进展。
12月26日的BALF NGS回报金葡菌和洋葱伯克霍尔德菌,后续药敏试验提示此金葡菌为MRSA,但考虑现阶段感染仍然处于可控范围内,遂选择在抗感染基础上加强了抗炎治疗。12月27日将地塞米松加量至10 mg,并且加用巴瑞替尼;加用伏立康唑预防继发真菌感染。考虑患者病变短期内可能不会得到明显改善,后续有继发VAP的可能,所以在入ICU第5天给患者气管切开。可以发现,增强抗炎治疗后,患者CRP和血清铁蛋白均呈下降趋势,但患者12月30日胸部X线片显示渗出有所增加,患者氧合指数改善并不明显。
IgA 385 mg/dl(↑)(68~378);C4 11.5 mg/dl(↓)(16~47);余未见异常。
CD3+T细胞:(12月25日)265 cell/μl(↓)(835~2217)→(12月28日)330 cell/μl(↓)→(12月30日)311 cell/μl(↓)→(1月4日)255 cell/μl(↓)。
CD4+T细胞:(12月25日)187 cell/μl(↓)(395~1264)→(12月28日)264 cell/μl(↓)→(12月30日)245 cell/μl(↓)→(1月4日)210 cell/μl(↓)。
顺应性:(12月22日)41 ml/cmH2O,(12月24日)45 ml/cmH2O。
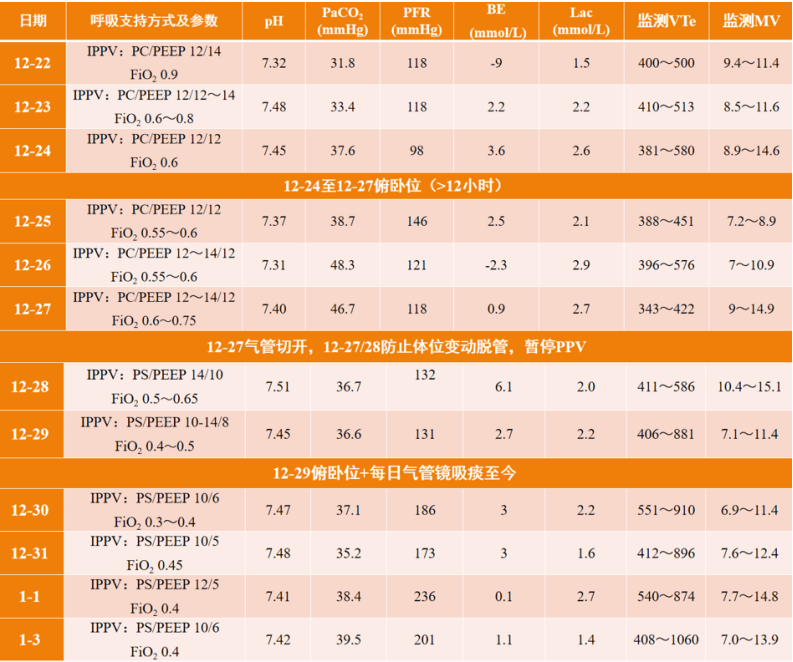
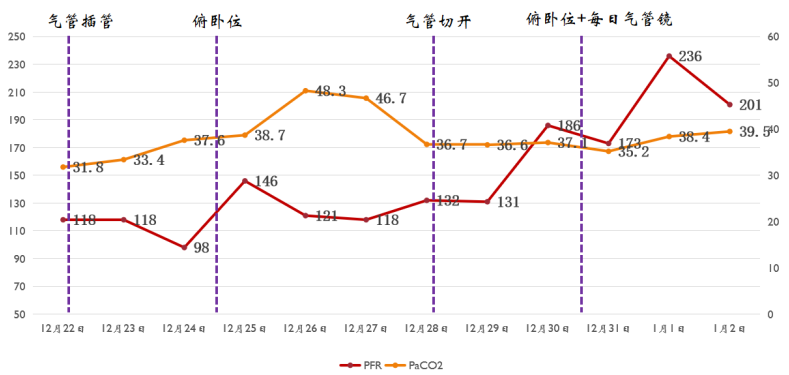
3. 循环方面
(1)心梗四项变化趋势
心电图:Ⅱ度Ⅰ型房室传导阻滞,HR 89次/min;窦性心动过缓,HR 45~59次/min,QT间期延长。间断给予阿托品静推和异丙肾上腺素泵入,心内科会诊建议待病情平稳后完善Holter检查。
入院后液体管理目标以±500 ml之间为主,12月29日患者自主尿量有所恢复,12月30日为观察患者肾脏恢复情况,CRRT下机,给予利尿剂后,尿量可达800 ml左右。
肝功能:AST、ALT、TBIL、DBIL基本正常范围。
双下肢静脉超声:12月23日双下肢深静脉未见明显血栓;12月28日右侧小腿肌间静脉静脉血栓形成。患者入院后予以预防性抗凝治疗,由于小腿肌间静脉血栓伴血小板下降,考虑有新发血栓形成导致的消耗状态,所以低分子肝素加量,但患者镜下血痰明显增加,血红蛋白缓慢下降,所以目前仍维持低分子肝素预防性抗凝。
目前情况
新冠核酸CT值>30;BALF MRSA、洋葱伯克霍尔德菌。
体温正常,WBC/PCT偏高(14.75×109/L/2.4ng/ml),LYM 0.27×109/L,气管镜下脓血痰较前略减少,但黏膜仍有活动性渗血。
持续CRRT,目标±500 ml;cTnI偏高;心脏超声未见明显异常。
肾功未完全恢复,尿量400~500 ml/d;肝功能基本正常;肠内营养支持;血糖控制等。
经验&教训
1. 教训
关于抗感染治疗时机,结合病毒感染后的致病机制,在病程中期(7~12天,起病平均14天左右时),相当于入ICU的前5天,应该在谨慎评估感染以及针对性抗感染治疗过程中,开启足量、联合的抗炎治疗。药物主要是以40~80 mg甲强龙或6~10 mg地塞米松联合托珠单抗。在病程后期(14天左右,即入ICU后1周左右),应再次评估有无继发感染的问题,进而调整抗炎治疗策略。同时,还应评估早期气管切开以及应用俯卧位,加强气管镜吸痰等痰液引流措施,改善患者继发感染。
专家讨论
对于重症新冠患者的救治,我们都面临着同样的问题,我们也从临床实践中总结了一些经验。在重症新冠患者救治中,“果断”非常重要。为了尽量避免出现医疗挤兑,对于重症新冠高危人群,如高龄、有基础疾病、妊娠、肥胖、长期应用免疫抑制剂的患者、接触人群有出现新冠病毒感染,在药物可及的情况下,即使没有检测抗原和核酸,一旦出现症状就应开始使用抗病毒药物。在改善重症新冠患者转归中,抗炎治疗非常重要。炎症风暴的有效时间窗比较短,一旦错过最佳治疗时间,后续可能面临抗炎及抗感染之间如何平衡的问题。抗炎的窗口期往往是在高危人群起病1周左右,如果体温没有恢复正常,胸闷、气短症状持续7~8天,即使肺部影像学看上去并不严重,个人认为还是要果断地足量使用抗炎药物。有些患者入院或入ICU后已经错过了最佳的抗炎时期,所以在后期,抗感染(合并感染)不可避免。重症新冠患者的个体化非常强,例如有基础疾病及器官移植患者,其自身清除病毒的能力差异非常大,在发病5~7天后是否就不能使用抗病毒药物?答案是可以使用,但由于后期用药种类多,需要我们注意药物之间的相互作用。对于托珠单抗,个人认为要尽早和足量,临床晚用2天,患者预后就存在很大差异。我们第一例使用托珠单抗的患者,当日下午由当地医院转入,氧饱和度70%,病情很重,激素已经使用多天,当天下午使用了托珠单抗,第二天氧饱和度升高至90%。对于重症患者,建议在激素治疗基础上尽早加入托珠单抗,该药物相对比较安全。巴瑞替尼起效相对较慢。中期果断抗炎极为重要,这也决定了患者后期的预后。

张帅
中日友好医院呼吸与危重症医学科主治医师,医疗组长,长期致力于肺栓塞、肺动脉高压等肺血管疾病的临床与转化医学研究,入选中日友好医院“菁英计划”人才培育工程,第一作者发表SCI论文10篇,核心期刊论文多篇,参编/译呼吸与危重症医学专著2部

黄琳娜
中日友好医院呼吸与危重症医学科主治医师,医疗组长,国家认证的PCCM专科医师,参与科技部国家重点研发计划1项,以重症感染为主要研究方向,建立及管理科室重症流感、重症侵袭性曲霉菌感染、重症肺孢子菌肺炎及免疫抑制肺炎数据库,熟练掌握多种呼吸系统常见疾病的诊治,尤其是呼吸衰竭的救治、呼吸支持技术等ICU多种脏器监护与支持技术,以第一作者及通讯作者发表SCI论文8篇,中文核心期刊论文多篇
 后可发表评论
后可发表评论

相关推荐
1
詹庆元教授|关于制作「重症COVID-19临床救治专家推荐意见临床实施简表」的推荐及说明
7465
2
翟振国教授|重症新冠患者的抗凝治疗:如何平衡血栓和出血的风险
6756
3
重症新冠病毒感染的呼吸支持治疗
4569
4
COVID-19炎症因子及免疫失衡指标&共感染
4228
5
重症新冠合并感染的临床流行病学
3680
6
新冠病毒肺部感染影像学特征及动态演变
3556
7
我国Omicron变异株所致重症COVID-19的流行病学
3422
8
重症新冠肺炎的临床表现
3394
9
詹庆元教授:重症新冠感染救治的几个关键问题
3208
10
重症COVID-19病例分享-7
3187



友情链接
联系我们
 公众号
公众号
 客服微信
客服微信