登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
单位:国家呼吸医学中心 中日友好医院呼吸与危重症医学科MICU
1
充分的氧供取决于动脉血氧含量和全身灌注情况(心排量)。在ECMO支持期间,影响灌注的因素会一直存在,包括右室功能不全、出血、低血容量、血管张力降低引起的休克等。VV-ECMO对循环没有直接改善作用,但可以通过纠正低氧、二氧化碳潴留相关的酸中毒,改善血管张力;也可以通过改变胸腔内压力,间接减少对循环的影响,尤其是存在右室功能不全时。
表1 体外膜肺氧合时各监测方式的可靠性
注:LVOT VTI:左室流出道速度时间积分;PPV:脉压变异度;SVV:每搏量变异度
ECMO时应该在固定流量的前提下评估心脏超声,尤其是VA-ECMO,因为不同的流量下左室负荷的降低程度有所不同。在固定流量的前提下,除测量左房左室大小外,反映容量过负荷的指标包括:①左室增大后继发的主动脉瓣、二尖瓣反流;②主动脉增宽;③左室舒张功能进一步恶化;④左室收缩功能下降(超过最适初长度)等。心脏超声不仅有助于判断容量状态,还可以直观地展示心脏收缩/舒张功能,以及主动脉瓣是否开瓣、左室前向血流、心腔内血栓形成等。床旁超声需观察的指标见表2。
2
1. 补液试验
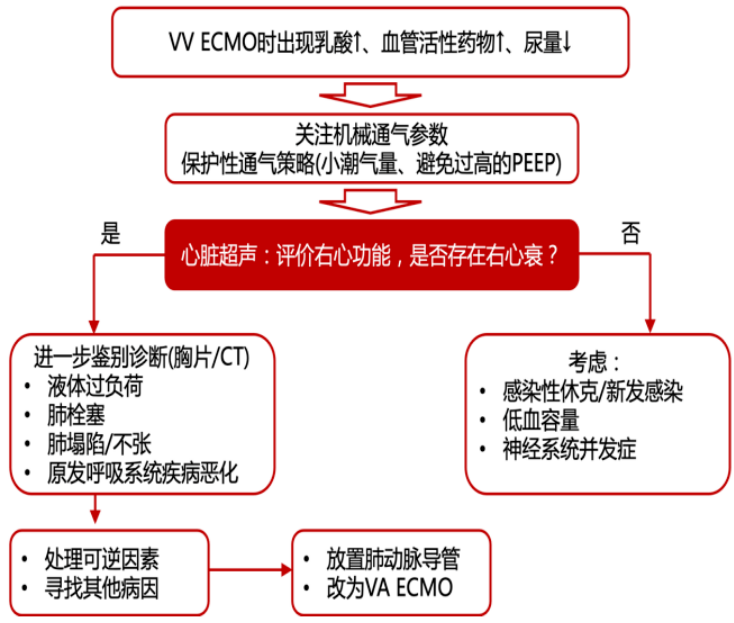
优化容量状态对于改善心功能也有一定帮助,在VA-ECMO时出现循环波动时更需要及时而仔细地进行心脏超声检查,根据超声调整液体策略或予以其他强心、调整ECMO流量等治疗。观察指标见前述表2。
3
在ECMO支持时,很多ICU常规的血流动力学监测方法失去了准确性。因此,在出现血流动力学波动时,对指标错误的解读可能导致治疗失败。应在充分了解其原理和病生理基础上结合临床进行分析解读,很多指标可以协助临床决策。
参考文献 [1] Siriwardena M, Dozois M, Fan E, et al. Hemodynamic Aspects of Veno-Arterial Extracorporeal Membrane Oxygenation for Cardiac Support: A Worldwide Survey[J]. ASAIO J, 2020, 66(5):489-496. doi:10.1097/MAT.0000000000001024 [2] Krishnan S, Schmidt G A. Hemodynamic Monitoring in the Extracorporeal Membrane Oxygenation Patient[j]. Curr Opin Crit Care, 2019, 25(3):285-291. doi:10.1097/MCC.0000000000000602 [3] Russ M, Steiner E, Boemke W, et al. Extracorporeal Membrane Oxygenation Blood Flow and Blood Recirculation Compromise Thermodilution-Based Measurements of Cardiac Output[J]. ASAIO J, 2022, 68(5):721-729. doi:10.1097/MAT.0000000000001592 [4] Lahmer T, Mayr U, Rasch S, et al. In-Parallel Connected Intermittent Hemodialysis through Ecmo Does Not Affect Hemodynamic Parameters Derived from Transpulmonary Thermodilution[J]. Perfusion, 2017, 32(8):702-705. doi:10.1177/0267659117707816 [5] Alvarado Sánchez J I, Caicedo Ruiz J D, Diaztagle Fernández J J, et al. Predictors of Fluid Responsiveness in Critically Ill Patients Mechanically Ventilated at Low Tidal Volumes: Systematic Review and Meta-Analysis[J]. Ann Intensive Care, 2021, 11(1):28. doi:10.1186/s13613-021-00817-5 [6] Pinsky M R. My Paper 20 Years Later: Effect of Positive End-Expiratory Pressure on Right Ventricular Function in Humans[J]. Intensive Care Med, 2014, 40(7):935-941. doi:10.1007/s00134-014-3294-8 [7] Zhang Z, Ni H, Qian Z. Effectiveness of Treatment Based on Picco Parameters in Critically Ill Patients with Septic Shock and/or Acute Respiratory Distress Syndrome: A Randomized Controlled Trial[J]. Intensive Care Med, 2015, 41(3):444-451. doi:10.1007/s00134-014-3638-4 [8] Via G, Tavazzi G, Price S. Ten Situations Where Inferior Vena Cava Ultrasound May Fail to Accurately Predict Fluid Responsiveness: A Physiologically Based Point of View[J]. Intensive Care Med, 2016, 42(7):1164-1167. doi:10.1007/s00134-016-4357-9 [9] Peris A, Lazzeri C, Cianchi G, et al. Clinical Significance of Echocardiography in Patients Supported by Venous-Venous Extracorporeal Membrane Oxygenation[J]. J Artif Organs, 2015, 18(2):99-105. doi:10.1007/s10047-015-0824-2 [10] Bunge J J H,Caliskan K, Gommers D, et al. Right Ventricular Dysfunction During Acute Respiratory Distress Syndrome and Veno-Venous Extracorporeal Membrane Oxygenation[J]. J Thorac Dis, 2018, 10(Suppl 5):S674-S682. doi:10.21037/jtd.2017.10.75 作者简介 冯莹莹
【注:本文仅用于学术内容的传播和交流,不用于任何商业和推广】
 后可发表评论
后可发表评论




友情链接
联系我们
 公众号
公众号
 客服微信
客服微信