登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
作者:吴小静
单位:中日友好医院呼吸与危重症医学科
下呼吸道感染是全球主要死亡原因之一。在2016年WHO公布的全球十大死亡原因中,慢阻肺排在第三位,下呼吸道感染排在第四位[1]。慢阻肺发展至晚期,很多患者会因合并重症下呼吸道感染而死亡。此外,肺癌、糖尿病等疾病患者最终也都是因感染而死亡。
SCAP的诊断标准
SCAP的病原学特点
西班牙一项全国多中心研究发现,在SCAP患者中,病原学的检出率约为54%,其中以肺炎链球菌、葡萄球菌为主,铜绿假单胞菌也占一定的比例,而军团菌和病毒亦不少见[3]。一项欧洲多国参与的多中心研究发也总结了SCAP患者的病原学情况,发现肺炎链球菌和葡萄球菌占比最高,军团菌和病毒不少见,尤其是军团菌[4]。
引起SCAP的病原微生物种类繁多。在非免疫抑制SCAP患者中,最常见的3种病原体分别是鼻病毒(9%)、流感病毒(6%)和肺炎链球菌(5%),即使是同一种病原体,也可能因为编码不同的毒力因子而影响下呼吸道感染的疾病进程[5]。
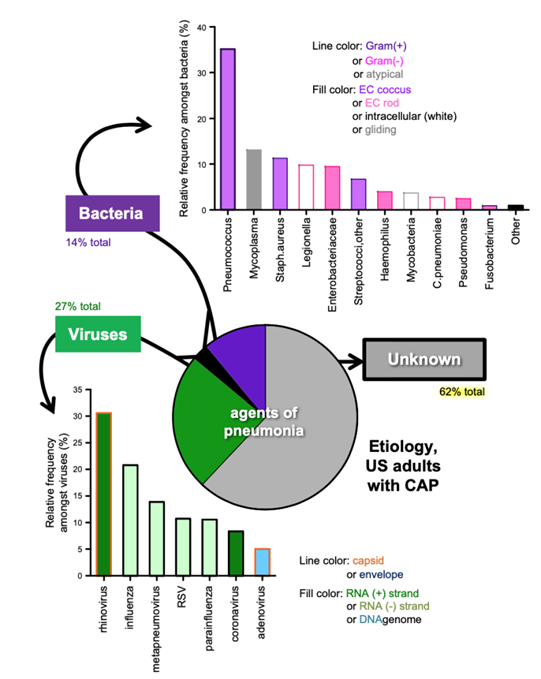
图源:Physiol Rev, 2018, 98(3):1417-1464.
我中心从2017年至2019年12月纳入238例SCAP患者,病原学排在首位的是流感病毒,其次是曲霉,军团菌占比接近8%,非典型病原体约占13%。流感病毒比例偏高,这可能与我中心的数据偏倚有关,在2017、2018、2019连续三年的流感季,我中心承担了很多外地重症流感患者的转运救治工作。而曲霉占比较高可能也与此有关。在曲霉感染的诊断标准中,宿主因素至关重要,包括免疫抑制宿主,而重症流感患者也考虑是免疫抑制宿主,是合并曲霉感染的高发人群。
在SCAP诊断及经验性抗感染治疗中,必须要注意患者的免疫情况,因为免疫抑制患者更易累及下呼吸道及肺泡腔,也更易出现弥漫性病变,而且进展会更加迅速,更易出现呼吸衰竭,需要入住ICU,此类患者可能同时合并多种病原感染(如细菌、病毒、真菌、结核分枝杆菌等),如果不能激活有效的获得性免疫,则可能导致天然免疫过度激活,加重肺损伤。在免疫正常患者中,病毒感染本身即可成为免疫抑制的因素。
当前发布的CAP指南均将免疫抑制患者排除在外,所有关于CAP的指南,对于经验性抗感染治疗的推荐,实际上针对的都是免疫功能正常患者,但是免疫抑制患者数量越来越大,关于免疫抑制患者CAP的病原学也更加复杂。
免疫抑制
免疫抑制并没有统一的概念,2020年Chest发表了一篇关于免疫抑制患者CAP治疗的专家共识,该共识提出了免疫抑制的定义[6]。原发性免疫缺陷患者、活动性肿瘤或者发生CAP 1年以内的肿瘤(除外局部皮肤癌或早期癌症)患者、恶性肿瘤化疗患者、HIV患者(CD4 T淋巴细胞<200/μl或占比<14%)、实体器官移植术后患者、骨髓干细胞移植术后患者、口服激素患者(等效强的松剂量≥20 mg/d,同时疗程≥14天,或等效强的松总量>700 mg)、接受生物制剂或免疫抑制剂治疗的患者,都认为是免疫抑制患者。长期口服激素、骨髓移植、化疗是引起免疫抑制SCAP排名前三位的基础疾病。
免疫抑制的原因往往并不单一。研究显示,47.9%的患者存在一个以上免疫抑制危险因素;活动性实体肿瘤与化疗、粒细胞缺乏,类固醇激素使用与器官移植术后、生物制剂使用等危险因素之间均存在交叉重叠。一项研究纳入600多例免疫抑制患者,其中约有50%的患者只存在一种免疫抑制因素,其余患者均存在2个以上免疫抑制因素[7]。
图源:Clin Infect Dis, 2019, 68(9):1482-1493.
我中心对2017年1月1日至2019年12月31日入住MICU的SCAP合并免疫抑制患者的病原学分布进行回顾性分析,共收集119例患者的临床资料,结果显示,免疫抑制患者最常见的基础疾病是长期口服激素,其次是血液系统疾病和恶性肿瘤,当然这其中也存在一些中心偏倚。
当出现肺部感染时,有多个肺外器官帮助抵抗这种感染。例如,骨髓紧急造血,帮助感染部位迅速募集中性粒细胞;肝脏合成和分泌大量急性期循环蛋白(APP),增强吞噬作用;脾的边缘区B细胞产生的IgM对一些呼吸道病原体特别重要,来源于脂肪细胞的瘦素信号传导对于多种肺部感染小鼠模型的最佳免疫防御至关重要;肠黏膜是一个免疫丰富的环境,还在肠道外的组织部位(包括肺)产生免疫学后果。
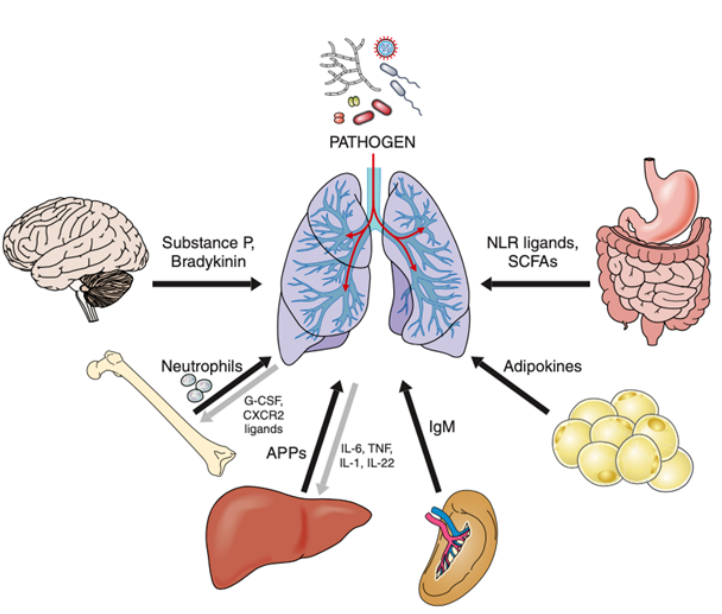
图源:Physiol Rev, 2018, 98(3):1417-1464.
免疫抑制与非免疫抑制CAP病原学
图源: Clin Infect Dis, 2022, ciac005.
我中心SCAP数据显示,非免疫抑制患者流感病毒感染比例高于免疫抑制患者,而免疫抑制患者CMV感染发病率显著高于非免疫抑制患者,免疫抑制患者肺孢子菌感染发病率显著高于非免疫抑制患者,非免疫抑制患者非典型病原体感染发病率显著高于免疫抑制患者。需要强调的是,免疫抑制患者混合感染的发生率显著高于非免疫抑制患者。
不同基础疾病的病原学风险
不同基础疾病患者的病原学风险存在一定差异。艾滋病、血液系统肿瘤患者是真菌感染的高危人群,营养不良患者是结核分枝杆菌感染的高危人群,血液系统肿瘤患者SCAP多合并非流感病毒感染。基础疾病无肺受累的免疫抑制SCAP患者感染肺孢子菌的概率更高。肺受累的基础疾病包括间质性肺病、结缔组织病引起的肺受累、肺癌、肺移植术后;无肺部受累组患者发生肺孢子菌感染风险显著高于肺部受累组(64.3% vs 44.2%,P=0.046)。
不同免疫抑制类型患者所特有的SCAP病原体,例如,粒缺患者首先考虑铜绿假单胞菌和曲霉感染的可能,艾滋病患者考虑肺孢子菌和结核分枝杆菌感染风险,T细胞耗竭(抗胸腺细胞球蛋白、阿伦单抗)患者考虑肺孢子菌、隐球菌以及单纯疱疹病毒感染,低丙种球蛋白血症患者考虑呼吸道合胞病毒感染,使用神经磷酸酶抑制剂(环孢素、他克莫司)患者要考虑诺卡菌或曲霉感染,使用雷帕霉素抑制剂的患者需考虑隐球菌或曲霉感染风险,使用糖皮质激素的患者首先考虑铜绿假单胞菌及肺孢子菌感染风险。
免疫抑制患者经验性覆盖条件致病微生物的指征
(5)免疫抑制患者的经验性抗诺卡菌指征,①宿主特征:实体器官移植术后(肺、心脏、肝脏),造血干细胞移植术后,未接受TMP-SMX预防治疗。②临床特征:肺炎合并肺脓肿或脑脓肿。③治疗推荐:TMP-SMX 15~20 mg/(kg·d)的甲氧苄啶。
(6)免疫抑制患者的经验性抗CMV指征:①宿主特征:肺移植术后,造血干细胞移植术后。②临床特征:双肺弥漫性磨玻璃影伴小叶间隔增厚。③治疗推荐:更昔洛韦:5 mg/kg q12h。
(7)免疫抑制患者的经验性抗水痘-带状疱疹病毒指征,①临床特征:双肺多发结节浸润伴水疱性皮疹。②治疗推荐:阿昔洛韦10~15 mg/kg q8h。
小结
参考文献
[1] Bcheraoui C E, Mokdad A H, Dwyer-Lindgren L, et al. Trends and Patterns of Differences in Infectious Disease Mortality Among US Counties, 1980-2014[J]. JAMA, 2018, 319(12):1248-1260.
[2] Mandell L A, Wunderink R G, Anzueto A, et al. Infectious Diseases Society of America; American Thoracic Society Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults[J]. Clin Infect Dis, 2007, 44(suppl 2):S27-S72.
[3] Cillóniz C, Ewig S, Ferrer M, et al. Community-acquired polymicrobial pneumonia in the intensive care unit: aetiology and prognosis[J]. Crit Care, 2011, 15(5):R209.
[4] Walden A P, Clarke G M, McKechnie S, et al. Patients with community acquired pneumonia admitted to European intensive care units: an epidemiological survey of the GenOSept cohort[J]. Crit Care, 2014, 18(5):R58.
[5] Quinton L J, Walkey A J, Mizgerd J P. Integrative Physiology of Pneumonia[J]. Physiol Rev, 2018, 98(3):1417-1464.
[6] Ramirez J A, Musher D M, Evans S E, et al. Treatment of Community-Acquired Pneumonia in Immunocompromised Adults: A Consensus Statement Regarding Initial Strategies[J]. Chest, 2020, 158(5):1896-1911.
[7] Pasquale M F, Sotgiu G, Gramegna A, et al. Prevalence and Etiology of Community-acquired Pneumonia in Immunocompromised Patients[J]. Clin Infect Dis, 2019, 68(9):1482-1493.
[8] Sousa D, Justo I, Domínguez A, et al. Community-acquired pneumonia in immunocompromised older patients: incidence, causative organisms and outcome[J]. Clin Microbiol Infect, 2013, 19(2):187-192.
[9] Certan M, Garcia Garrido H M, Wong G, et al. Incidence and Predictors of Community-Acquired Pneumonia in Patients With Hematological Cancers Between 2016 and 2019[J]. Clin Infect Dis, 2022, ciac005.
 后可发表评论
后可发表评论




友情链接
联系我们
 公众号
公众号
 客服微信
客服微信