登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
作者:詹丹婷,王凌伟
单位:深圳市呼吸疾病研究所
移植物抗宿主病(graft-versus-host disease,GVHD)特指发生在异基因造血干细胞移植(allogeneic hematopoietic stem cell transplantation,allo-HSCT)术后的免疫性疾病,发生率为30%~70%,严重影响allo-HSCT术后患者的存活率及生活质量,可累及全身多个系统或器官,呼吸系统是最常见的受累系统之一。部分患者因咳嗽、气促首诊于呼吸内科,可能仅诊断为支气管扩张甚至慢性阻塞性肺疾病而延误了原发病的诊治,是HSCT远期失败的最重要的病因之一。本文旨在总结GVHD的呼吸系统临床表现、影像学特点和诊断标准,以期提高呼吸科医生对此病的认识,提高早期诊断率。
一、流行病学
aGVHD是影响移植后非复发死亡的主要因素[1];cGVHD是allo-HSCT后受者在重建供者免疫过程中,来源于供者的淋巴细胞攻击受者脏器产生的临床病理综合征,是移植后主要并发症之一,发生率为30%~70%[2]。有研究使用T细胞耗竭和移植后环磷酰胺等预防策略,cGVHD的发生率可降至10%~15%[3-6]。但多数allo-HSCT患者即使接受GVHD预防,cGVHD的发生率仍高达30%~50%[7],是导致移植患者生活质量下降、移植失败的最主要原因之一。
二、GVHD临床表现
aGVHD常累及皮肤、胃肠道及肝脏,近年来也有累及胸腺、肺等的报道[8]。在所有allo-HSCT患者中,30%~50%发生aGVHD(Ⅰ~Ⅳ级),14%发生严重aGVHD(Ⅲ~Ⅳ级)[9]。
cGVHD最常累及部位为皮肤,其次为肝脏、眼部、肺部、口腔、肠道及血液系统,发生率为30%~70%[10]。临床上可表现为皮肤异色病、皮肤扁平苔藓样变、皮肤硬化样变、皮肤硬化性苔藓样变;口腔扁平苔藓样变、生殖器扁平苔藓样变、硬化性苔藓样变(女性阴道瘢痕或阴蒂/阴唇溃疡、男性包茎或尿道瘢痕/狭窄);食管网格、食管中上1/3狭窄;闭塞性细支气管炎、筋膜炎、继发于筋膜炎、硬化的关节僵硬和挛缩、口腔干燥、黏液腺囊肿、黏膜萎缩、溃疡或假膜;眼结膜新发干燥、沙砾感、疼痛感、瘢痕性结膜炎、干眼症和点状角膜病;生殖道糜烂、龟裂、溃疡;肌炎/多发性肌炎等。cGVHD早期征象不典型,一旦出现晨僵、皮肤感觉异常、肌肉酸痛、不明原因低热、乏力或活动后喘息、不明原因消瘦、眼涩、口干、味觉异常、肝肾功能异常、感觉或运动轻度障碍、大便性状改变及生殖系统异常变化等征象均需警惕cGVHD的可能[2]。
三、GVHD的高危因素
表1 GVHD常见的危险因素
四、GVHD呼吸系统的影像学特征
GVHD呼吸系统表现常见有闭塞性细支气管炎综合征(bronchiolitis obliterans syndrome,BOS)、弥漫性肺泡出血、植入综合征、特发性肺炎综合征、闭塞性细支气管炎伴机化性肺炎(bronehiolitis obliterans organizing pneumonia,BOOP)、肺血管内细胞溶解性栓子形成等[15]。间质性肺病属于HSCT术后并发症,3年累积发生率为5%。但是否属于cGVHD尚有争议[16]。研究表明,allo-HSCT非感染性呼吸系统并发症患者总生存率较低,BOS与移植患者预后不良有关,2年生存率为44%,5年生存率为13%[17]。
图1 52岁的女性植入综合征
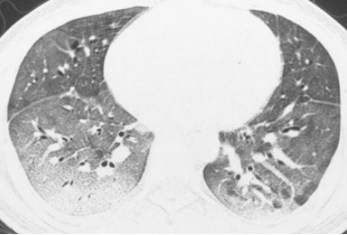
图2 27岁男性IPS患者
图3 IPS患儿肺部HRCT
图4 45岁男性急性髓系白血病患者
注:在allo-HSCT术后6个月后出现呼吸困难。A. 胸部CT显示支气管周围磨玻璃样改变;B. 1个月的随访CT显示疾病进展,磨玻璃样改变的范围增加、新进展的网格影及铺路石影、明显牵拉性支气管扩张[22]。
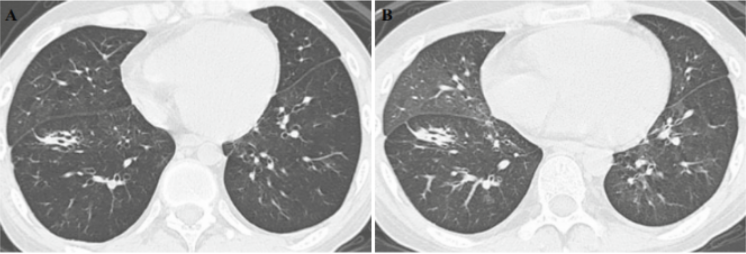
图6 16岁男性诊断移植后OP
回顾性研究[23]发现HSCT后间质性肺疾病(ILD)对应几种组织学模式,如OP和非特异性间质性肺炎、弥漫性肺泡损伤、淋巴细胞性间质性肺炎和胸膜实质性肺炎纤维弹性增生症。尤其需要注意的是,几乎所有病例组织学上呈现肺间质性改变与BO并存。故移植后ILD的原因不除外与环境、药物或遗传因素相关,尤其是allo-HSCT受者服用了多种可诱发ILD的药物[16]。
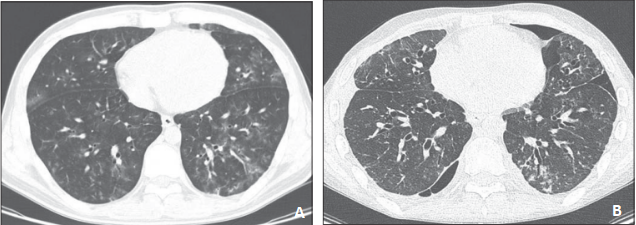
图7 24岁男性行HSCT治疗急性髓系白血病后出现呼吸困难
五、GVHD肺损伤的诊断标准[12,15]
满足以下4条标准即可诊断GVHD-BOS:
对于发育期少年儿童,肺功能指标以同年龄的肺功能百分位为准。病情严重而无法进行肺功能检查、因胸廓漏气综合征而不适合进行肺功能检查的患者,可用六分钟步行试验进行病情评估。
六、总结
参考文献(向下滑动查看全部文献)
[1] Yong K, Wilson W, de Tute R M, et al. A prognostic score for acute graft-versus-host disease based on biomarkers: a multicentre study[J]. Lancet Haematol, 2015, 2(1):e21-e9.
[2] 中华医学会血液学分会造血干细胞应用学组,中国抗癌协会血液病转化委员会. 慢性移植物抗宿主病(cGVHD)诊断与治疗中国专家共识(2021年版)[J]. 中华血液学杂志, 2021, 42(4):11.
[3] Kröger N, Solano C, Wolschke C, et al. Antilymphocyte Globulin for Prevention of Chronic Graft-versus-Host Disease[J]. N Engl J Med, 2016, 374(1):43-53.
[4] Bleakley M, Heimfeld S, Loeb K R, et al. Outcomes of acute leukemia patients transplanted with naive T cell–depleted stem cell grafts[J]. J Clin Invest, 2015, 125(7): 2677-2689.
[5] Luznik L, O'Donnell P V, Symons H J, et al. HLA-Haploidentical Bone Marrow Transplantation for Hematologic Malignancies Using Nonmyeloablative Conditioning and High-Dose, Posttransplantation Cyclophosphamide[J]. Biol Blood Marrow Transplant, 2008, 14(6):641-650.
[6] Mielcarek M, Furlong T, O'Donnell P V, et al. Posttransplantation cyclophosphamide for prevention of graft-versus-host disease after HLA-matched mobilized blood cell transplantation [J]. Blood, 2016, 127(11): 1502-1508.
[7] Kitko C L, Pidala J, Schoemans H M, et al. National Institutes of Health Consensus Development Project on Criteria for Clinical Trials in Chronic Graft-versus-Host Disease: IIa. The 2020 Clinical Implementation and Early Diagnosis Working Group Report[J]. Transplant Cell Ther, 2021, 27(7):545-557.
[8] Liu Q F, Luo X D, Ning J, et al. Association between acute graft versus host disease and lung injury after allogeneic haematopoietic stem cell transplantation[J]. Hematology, 2009, 14(2):63-72.
[9] Zeiser R, Blazar B R. Acute Graft-versus-Host Disease - Biologic Process, Prevention, and Therapy[J]. N Engl J Med, 2017, 377(22):2167-2179.
[10] 陈东阳, 张红宾, 汪晶, 等. 血液病患者异基因造血干细胞移植后慢性移植物抗宿主病的临床特征及其对预后的影响[J]. 白血病·淋巴瘤, 2022, 31(6):330-337.
[11] 周婷, 肖坤, 闫鹏, 等. 异基因造血干细胞移植术后肺部移植物抗宿主病的临床特点及细胞免疫特征[J]. 中华结核和呼吸杂志, 2019, 42(12):938-940.
[12] Williams K M, Inamoto Y, Im A, et al. National Institutes of Health Consensus Development Project on Criteria for Clinical Trials in Chronic Graft-versus-Host Disease: I. The 2020 Etiology and Prevention Working Group Report[J]. Transplant Cell Ther, 2021, 27(6):452-466.
[13] Kanda J, Nakasone H, Atsuta Y, et al. Risk factors and organ involvement of chronic GVHD in Japan[J]. Bone Marrow Transplant, 2014, 49(2):228-235.
[14] 范祎, 李飞, 王秀丽, 等. 异基因造血干细胞移植后慢性移植物抗宿主病: 移植前肺功能对肺部受累的预测作用[J]. 中国血液流变学杂志, 2017, 27(3):241-246.
[15] 陈静, 徐应永. 移植相关肺部非感染性并发症的诊断与防治进展[J]. 中国实用儿科杂志, 2009, 24(10):756-760.
[16] Archer G, Berger I, Bondeelle L, et al. Interstitial lung diseases after hematopoietic stem cell transplantation: New pattern of lung chronic graft-versus-host disease?[J]. Bone Marrow Transplant, 2023, 58(1):87-93.
[17] Wolff D, Radojcic V, Lafyatis R, et al. National Institutes of Health Consensus Development Project on Criteria for Clinical Trials in Chronic Graft-versus-Host Disease: IV. The 2020 Highly morbid forms report[J]. Transplant Cell Ther, 2021, 27(10):817-835.
[18] 刘四喜, 文飞球. 植入综合征[J]. 中国小儿急救医学, 2022, 29(8):573-576.
[19] 胡晓霞, 王健民. 造血干细胞移植后的植入综合征[J]. 白血病·淋巴瘤, 2005, 14(4):251-254.
[20] Tanaka N, Kunihiro Y, Yujiri T, et al. High-resolution computed tomography of chest complications in patients treated with hematopoietic stem cell transplantation[J]. Jpn J Radiol, 2011, 29(4): 229-235.
[21] 钱娟, 张建, 宁铂涛, 等. 儿童造血干细胞移植后特发性肺炎综合征行肺移植一例[J]. 中华儿科杂志, 2021, 59(5):412-414.
[22] Song I, Yi C A, Han J, et al. CT findings of late-onset noninfectious pulmonary complications in patients with pathologically proven graft-versus-host disease after allogeneic stem cell transplant[J]. AJR Am J Roentgenol, 2012, 199(3):581-587.
[23] Bergeron A, Chevret S, Peffault de Latour R, et al. Noninfectious lung complications after allogeneic haematopoietic stem cell transplantation[J]. Eur Respir J, 2018, 51(5):1702617.
作者简介 深圳市人民医院 深圳呼吸疾病研究所住院医师 2016—2019年于深圳市人民院住院医师规范化培训 2019—2022年于深圳市人民院呼吸与重症医学科专科医师规范化培训并择优留院 专培期间以第一或共一发表SCI论文3篇 广东省病理生理学会呼吸分会秘书兼委员 深圳市呼吸疾病研究所副所长 南方科技大学医学院诊断学教研室主任 博士,教授,主任医师,博士生导师 2005年入选中国卫生部国际资源后备人才库人才 2010年德国柏林Evangelische Lungenklinik医院进修 中华医学会呼吸病学分会第十一届委员会委员 中国医学装备协会呼吸病学分会副主任委员 广东省呼吸内科质控中心副主任 深圳市医师协会呼吸医师分会会长 深圳市医学会呼吸病学分会副主任委员 深圳市医防融合项目呼吸项目组组长 科技部重大专项《慢阻肺动物模型病理机制解析及新靶标的发现》课题负责人
声明:
 后可发表评论
后可发表评论




友情链接
联系我们
 公众号
公众号
 客服微信
客服微信