登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
作者:赵志刚

重症患者对氧气的需求较高,但其生理功能无法满足这一需求,氧供与氧耗严重不匹配,此类患者往往存在血流动力学紊乱,心肺状态不稳定。此外,ECMO管路留置、气管插管等各种有创操作势必为患者带来疼痛,而且外界因素刺激也会导致患者出现焦虑、躁动、谵妄、睡眠障碍等问题,因此,ECMO患者镇痛镇静非常必要。

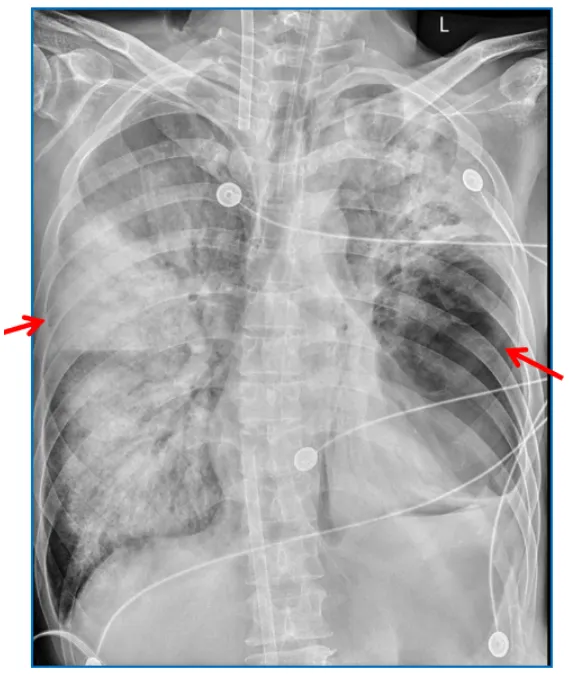
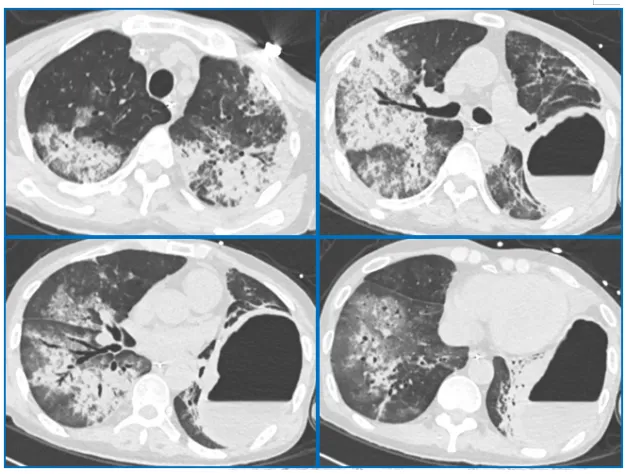
感染指标:WBC 4.9×109/L,NEU 4.37×109/L,NEU% 89.1%,LYM 0.39×109/L,LYM% 8.0%,Hb 102 g/L,PLT 384×109/L,CRP 117.44 mg/L,PCT 54.82 ng/ml。
肝功能:谷丙转氨酶63.2 U/L,谷草转氨酶59.1 U/L,总胆红素16.45 μmol/L,直接胆红素12.6 μmol/L。
心肌酶:肌钙蛋白I 158.3 ng/ml,肌红蛋白71.1 ng/ml,肌酸激酶40 U/L,肌酸激酶同工酶1 U/L,Pro-BNP 1360 pg/ml。
凝血功能:凝血酶原时间18.6 s,PT活动度45.4%,国际标准化比值1.65,活化部分凝血活酶时间44 s,凝血酶时间15.8 s,纤维蛋白原5.44 g/L,D-二聚体测定4.21 μg/ml,纤维蛋白原降解产物 17.39 μg/ml。
淋巴细胞:淋巴细胞 674/μl,白介素12P70 5.15 pg/ml,CD4+T淋巴细胞344/μl,CD8+T淋巴细胞217/μl。
阴性结果:肾功能,甲/乙流抗原,ANA+ENA,ANCA,G试验、GM试验,肿瘤标志物,血培养。
心脏超声:射血分数41%,每搏量62 ml,左室壁运动减低,左室收缩功能减低。
重症肺炎,急性呼吸窘迫综合征(ARDS),脓毒症,脓毒性休克,脓毒性心肌病,肝功能异常,高血压。
在实施镇静镇痛之前首先需要充分评估,尽量做到“无监测,勿镇静”。
镇静镇痛的评估方法分为主观和客观方法。客观方法主要为监测脑电双频指数(BIS)。这种方法在神经外科和麻醉科使用比较普遍。对于呼吸危重症患者,临床更多采用简单实用的评估量表,包括:①数字疼痛评分(NRS):分值范围0~10,0代表不痛,10代表疼痛难忍,由患者选择数字描述疼痛程度;②行为疼痛量表(BPS):通过患者的面部表情、上肢运动、机械通气顺应性判断疼痛程度;③重症监护疼痛观察量表(CPOT):通过患者的面部表情、动作、肌张力、发声/机械通气顺应性判断疼痛程度;④躁动镇静评分:包括Richmond躁动-镇静评分(RASS)和镇静-躁动评分(SAS)。
早期提出的eCASH理论对于ECMO患者依然适用。该理论强调以患者为核心,强调早期、舒适、简化并改进以患者为中心的护理;强调镇痛是起点,阿片类药物是镇痛的核心;强调减少不必要的过度镇静。
在ECMO支持过程中,我们也需要考虑影响药物浓度的因素,包括:①ECMO管路,例如膜式氧合器和聚氯乙烯管(PVC)管;②药物理化特性,包括亲脂性,蛋白结合力,分子大小,电离程度;③患者自身因素,例如年龄、血流动力学、肝肾功能等。
我们用logP【某物质在正辛醇(油)和水中的分配系数比值的对数值】来评估药物的亲脂性,logP越大代表药物亲脂性越高。文献表明,高亲脂性(logP>2)和高蛋白结合(>70%)的药物吸附在管路中,降低有效循环浓度,然而可以从管路中释放,在停止给药后继续发挥作用,此类药物需要调整给药剂量。低亲脂性(logP<1)和低蛋白结合(<30%)的药物不易受管路影响。介于二者之间的药物亲脂性(1<logP<2)低蛋白结合(30%~70%)需要进一步研究管路对药物剂量的影响。
研究显示,药物亲脂性由高到低依次为芬太尼、咪达唑仑、丙泊酚、劳拉西泮、右美托咪定、氢吗啡酮、吗啡。蛋白结合率由高到低依次为丙泊酚、咪达唑仑、右美托咪定、劳拉西泮、芬太尼、吗啡、氯胺酮、氢吗啡酮。按照logP<1、蛋白结合率<30%来看,氢吗啡酮无疑是镇痛药中的最佳选择。有研究比较了氢吗啡酮与芬太尼在ECMO患者中的镇痛效果,结果显示氢吗啡酮组7天内发生谵妄的天数短于芬太尼组,同时氢吗啡酮组的药物剂量也低于芬太尼组。另有研究评估肥胖患者接受VV-ECMO治疗时对镇静镇痛药物需求的特点。结果显示:7天内有31例患者的镇痛药物由芬太尼更换为氢吗啡酮,其中肥胖组有20例患者,非肥胖组有11例患者。研究认为,如果芬太尼剂量达到400 μg/h仍未达到镇痛效果,可考虑更换为氢吗啡酮。
氢吗啡酮在欧美国家也是首选的镇痛药物。但在我们国家目前还是芬太尼、瑞芬太尼应用比较广泛。在使用阿片类镇痛药物的同时, 也要警惕阿片类药物带来的不良反应, 例如免疫抑制、呼吸抑制、痛觉过敏、慢性疼痛综合征、成瘾依赖、抑制胃肠道蠕动等, 如果大剂量阿片类药物仍然不能满足患者的镇痛需求, 建议联合非阿片类药物, 如非甾体抗炎药、加巴喷丁、氯胺酮等。
Hohlfelder等研究探讨了丙泊酚在成人ECMO患者中的安全性。该研究纳入了43例患者,其中16例选用了丙泊酚。结果发现,丙泊酚组膜肺使用时间更长。因此认为丙泊酚对ECMO患者是安全的。这一结论可能与我们预想的不同。由于丙泊酚具有很强的亲脂性,在用药过程中,尤其是在后期,要减少其使用剂量,以预防丙泊酚输注综合征。Bakdach等研究分析了丙泊酚在ECMO期间抗凝和非抗凝患者中的安全性。研究纳入63例患者,29例(46%)患者接受丙泊酚作为镇静方案。结果表明丙泊酚与膜肺故障无关,即使在未抗凝情况下,丙泊酚也不会增加膜肺故障风险,膜肺故障唯一的预测因子为ECMO支持期间肝素诱导的血小板减少。
Patel等研究评估了VV-ECMO和VA-ECMO患者在初始ECMO插管期后每日镇痛和镇静药物剂量的需求。纳入26例患者,13例VV-ECMO,13例VA-ECMO。结果显示:VV组比VA组需要更高剂量的芬太尼,两组右美托咪定和丙泊酚使用剂量无显著差异。ECMO支持下芬太尼、右美托咪定和丙泊酚的中位日剂量在整个时间内并未显著增加,RASS评分-1~0的轻度镇静策略可行。也有文献列出了常用阿片类、非苯二氮卓类和苯二氮卓类等药物的蛋白结合率和亲脂性的对比,以及在ECMO支持期间是否需要增减药物,同时也强调了ECMO期间的注意事项——警惕这些药物的不良反应。
上机第1天:瑞芬太尼+咪达唑仑±右美托咪定,CPOT评分0~1分,RASS评分-5~-3分。此阶段镇痛镇静的目的是为了辅助完善气管镜及左侧胸腔穿刺,明确病原学。后经证实患者前期合并病毒感染,从灌洗液和左肺下叶引流的脓液中培养出口腔来源的链球菌。
上机第2~3天, 根据镇静镇痛评分加用丙泊酚; CPOT评分0~1分, RASS评分-5~-3分。此时患者采取俯卧位或高侧卧位, 加强引流。
上机第3~6天,必要时加入肌松剂。CPOT评分0~1分,RASS评分-2~0分。气管切开。患者病情逐渐稳定,逐渐降低镇静深度。
经过引流、抗感染、营养支持、康复锻炼等治疗和干预后,患者病情明显好转。
上机第7~8天, 减少咪达唑仑剂量, 丙泊酚过渡。CPOT评分0~1分, RASS评分-2~0分。
ECMO上机8天后成功撤离。使用右美托咪定减少患者谵妄和情绪波动, RASS评分0分。
经过治疗,患者乳酸水平逐渐下降,撤机后乳酸水平趋于正常(表1)。炎症指标如WBC、CRP、PCT下降并恢复正常(图3)。
表1 入院后患者血气分析指标变化情况
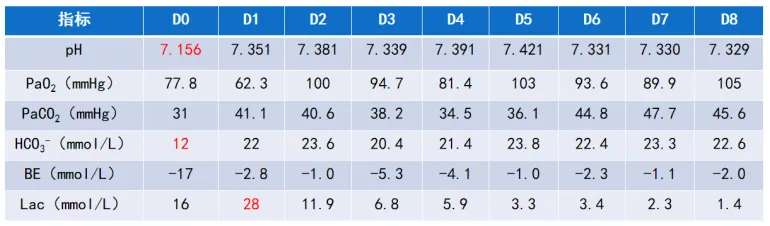
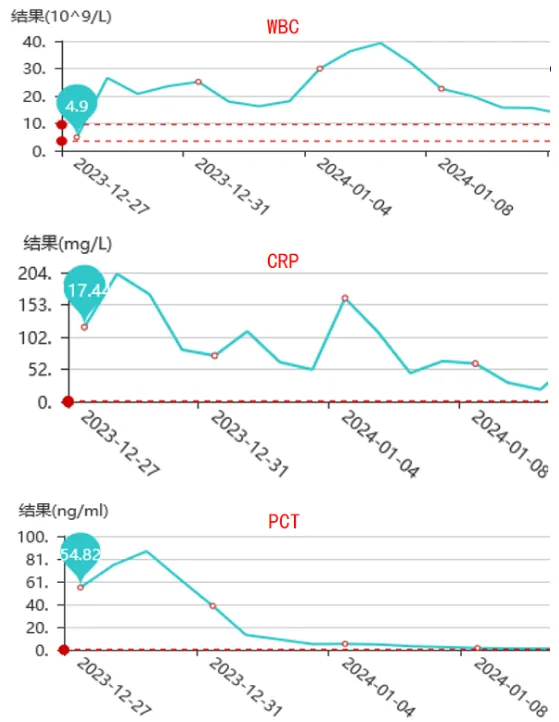
图3 患者炎症指标变化情况

结合相关文献,ECMO患者的镇静镇痛策略可分为以下步骤:
步骤六、肌松。如果深度镇静(例如,Richmond躁动镇静等级4或5)且伴有严重缺氧,可考虑开始使用神经肌肉阻滞剂而不是进一步增加镇静剂;在有恢复证据停止使用神经肌肉阻滞剂之前,不要减少镇静剂。

ECMO上机过程中药物影响因素很多,包括患者自身因素、药物因素和ECMO设备因素。不同文献的结果差异较大,临床实践与理论之间仍然存在一定的差距。迄今为止,还没有公认的ECMO镇静镇痛临床指南,目前大部分研究为单中心且样本量小,期望今后有更多多中心、大样本的临床研究来提供强有力的循证医学证据。另外,在药物选择过程中,药物可及性差异较大。因此,对于ECMO患者,我们更倾向于以目标为导向的个体化镇静镇痛策略。
参考文献
作者介绍
河南省人民医院呼吸与危重症医学科,主治医师,硕士研究生毕业于解放军总医院,主要从事重症感染、呼吸衰竭、脓毒症等危重症的诊断和治疗。
 后可发表评论
后可发表评论




友情链接
联系我们
 公众号
公众号
 客服微信
客服微信